题目内容
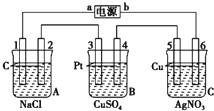 如图,通电5min后,电极5质量增加2.16g,回答:
如图,通电5min后,电极5质量增加2.16g,回答:(1)电源:a是
(2)电池电极反应,电极1:
考点:原电池和电解池的工作原理
专题:电化学专题
分析:通电5min后,电极5质量增加2.16g,说明电极5是阴极,得电子析出金属单质,所以a是电源的负极,b是电源的正极.
则1、3、5为阴极,发生还原反应,2、4、6发生氧化反应,结合离子放电顺序解答该题.
则1、3、5为阴极,发生还原反应,2、4、6发生氧化反应,结合离子放电顺序解答该题.
解答:
解:通电5min后,电极5质量增加2.16g,说明电极5是阴极,得电子析出金属单质,所以a是电源的负极,b是电源的正极.
(1)a为负极,A池为电解食盐水装置,1发生还原反应生成氢气,2发生氧化反应生成氯气,发生2Cl--2e-=Cl2↑,使湿润KI淀粉试纸变蓝;B池中4为阳极,发生氧化反应,电解方程式为2CuSO4+2H2O
2Cu+O2↑+2H2SO4,则溶液pH减小,
故答案为:负;2;4;减小;
(2)1为阴极,发生反应反应,电极方程式为2H++2e-=H2↑,4为阳极,发生氧化反应,电极方程式为4OH--4e-=2H2O+O2↑,
故答案为:2H++2e-=H2↑;4OH--4e-=2H2O+O2↑.
(1)a为负极,A池为电解食盐水装置,1发生还原反应生成氢气,2发生氧化反应生成氯气,发生2Cl--2e-=Cl2↑,使湿润KI淀粉试纸变蓝;B池中4为阳极,发生氧化反应,电解方程式为2CuSO4+2H2O
| ||
故答案为:负;2;4;减小;
(2)1为阴极,发生反应反应,电极方程式为2H++2e-=H2↑,4为阳极,发生氧化反应,电极方程式为4OH--4e-=2H2O+O2↑,
故答案为:2H++2e-=H2↑;4OH--4e-=2H2O+O2↑.
点评:本题考查电解知识,为高频考点,侧重于学生的分析能力的考查,注意把握电极方程式的书写,根据电极反应现象判断电源的正负极为解答该题的关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
“原子经济性”是“绿色化学”重要内涵.它主张在化学转化获取新物质的过程中充分利用每个原子,这样既能够充分利用资源,又能够防止污染.从“原子经济性”的角度考虑,以下转化最合理的是( )
| A、消除制硝酸工业尾气的氮氧化物污染:NO2+NO+2NaOH=2NaNO2+H2O,2NO2+2NaOH=NaNO2+NaNO3+H2O | ||||
B、制备Cu(NO3)2:2Cu+O2
| ||||
C、利用二氧化碳制造全降解塑料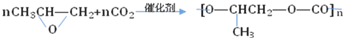 | ||||
D、用铜与浓硫酸共热制硫酸铜:Cu+2H2SO4(浓)
|
已知丙酮(C3H6O)通常是无色液体,不溶于水,密度小于1g?mL-1,要从水与丙酮的混合物里将丙酮分离出来,下列方法中最合理的是( )
| A、分液 | B、蒸馏 | C、过滤 | D、蒸发 |
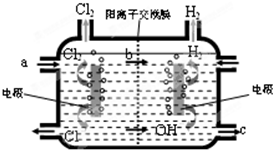 (1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为
(1)已知甲醇在常温下为液体,其热值为22.7kJ?g-1,则甲醇的标准燃烧热的热化学方程式为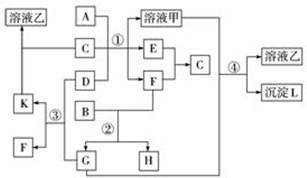 在图中表示的是有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)
在图中表示的是有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)