题目内容
19.研究物质的微观结构,有助于人们理解物质变化的本质.请回答:(1)C、N、O元素的第一电离能由大到小的顺序是N>O>C.
(2)A、B均为短周期金属元素.依据下表数据,
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
(3)①COCl2分子的结构式为
 ,COCl2分子内含有D(填标号);
,COCl2分子内含有D(填标号);A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键
(4)甲苯结构简式:
 ,其中C原子采用的轨道杂化方式有sp2、sp3.
,其中C原子采用的轨道杂化方式有sp2、sp3.(5)ClO3-离子的立体构型是三角锥形,写出一种与ClO3-互为等电子体的微粒的化 学式SO32-(IO3-BrO3-NCl3).
(6)比较C、Si、N元素形成简单的氢化物稳定性高低并说明理由稳定性:NH3>CH4>SiH4,因为键长N-H<C-H<Si-H,又键长越短,键能越大,所以稳定性
为NH3>CH4>SiH4.
分析 (1)同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,据此判断第一电离能大小顺序;
(2)由表中数据可知,A、B元素的第三电离能都剧增,故表现+2价,为第ⅡA族元素,B的第一电离能比A的小,故B为Mg元素,根据原子核外电子排布规律书写;
(3)共价单键是σ键,共价双键中一个是σ键一个是π键,COCl2分子内含2个C-Cl和1个C=O键;
(4)由结构式中的键和孤电子对数判断氮原子采用的杂化方式;
(5)根据价层电子对互斥理论来确定其空间构型;原子个数相等、价层电子数相等的微粒互为等电子体;
(6)共价键键长越短、键能越大,共价键越稳定,物质稳定性越强.
解答 解:(1)同一周期元素,元素的第一电离能随着原子序数增大而增大,但第IIA族、第VA族元素第一电离能大于其相邻元素,C、N、O元素处于同一周期且原子序数逐渐增大,N处于第VA族,所以第一电离能N>O>C;
故答案为:N>O>C;
(2)由表中数据可知,A、B元素的第三电离能都剧增,故表现+2价,为第ⅡA族元素,B的第一电离能比A的小,故B为Mg元素,原子的电子排布式为1s22s22p63s2;
故答案为:1s22s22p63s2;
(3)C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,所以D正确;
故答案为:D;
(4)甲苯分子中苯环碳原子原子采取sp2杂化,甲基碳原子采取sp3杂化;
故答案为:sp2、sp3;
(5)ClO3-中价层电子对个数=3+$\frac{1}{2}$(7+1-3×2)=4,且含有一个孤电子对,所以是三角锥型;等电子体具有相同的价电子数目和原子数目的微粒,所以与ClO3-互为等电子体的微粒有SO32-( IO3-BrO3-NCl3);
故答案为:三角锥形;SO32-( IO3-BrO3-NCl3);
(6)共价键键长越短、键能越大,共价键越稳定,物质稳定性越强,C、Si、N元素形成简单的氢化物中:因为键长N-H<C-H<Si-H,又键长越短,键能越大,所以稳定性
为NH3>CH4>SiH4;
故答案为:稳定性:NH3>CH4>SiH4;因为键长N-H<C-H<Si-H,又键长越短,键能越大,所以稳定性为NH3>CH4>SiH4.
点评 本题考查较为综合,涉及多个方面的知识,题目难度较大,本题注意元素周期律的递变以及对数据的分析和判断,学习中注重相关基础知识和解题方法的积累.

 53天天练系列答案
53天天练系列答案| A. | 30g C2H6中含有的共用电子对数为6NA | |
| B. | 1.0L 1.0mol•L-1Na3PO4水溶液中含有的氧原子数为4NA | |
| C. | 1 mol FeI2与足量氯气反应转移的电子数为3NA | |
| D. | 25℃时,1.0L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| A. | O2和O3 | B. | CO和CO2 | C. | H2O和H2O2 | D. | 24Mg和26Mg |
| A. | 离子晶体中一定含金属阳离子 | |
| B. | 只要含有金属阳离子的晶体就一定是离子晶体 | |
| C. | 分子晶体的熔点不一定比金属晶体的熔点低 | |
| D. | 在共价化合物分子中,各原子都形成8电子结构 |
| A. | pH=9.25、浓度均为0.1 mol•L-1的NH4C1、NH3•H2O混合溶液:c(NH4+)+c(H+)>c(NH3•H2O)+c(OH-) | |
| B. | 0.1mol/LH2SO4溶液与0.1mol/LNaOH溶液等体积混合:c(H+)═c(SO42-)+c(OH-) | |
| C. | 向0.10mol•L-1NaHSO3溶液中通NH3至pH=7:c(Na+)>c(SO32-)>c(NH4+) | |
| D. | CO2通入KOH溶液,当由水电离的H+浓度为10-7mol/L,一定存在:c(K+)=2c(CO32-)+c(HCO3-) |
| A. | A 原子最外层电子数比 B 原子的最外层电子数少 | |
| B. | A 原子电子层数比 B 原子的电子层数多 | |
| C. | 常温时,A能从酸中置换出氢,而B不能 | |
| D. | 1molA从酸中置换生成的 H2比 1mol B从酸中置换生成的 H2多 |
| A. | Na2O2 Al2(SO4)3 MgCl2 K2CO3 | |
| B. | BaCl2 Na2SO4 (NH4)2SO4 KOH | |
| C. | AgNO3 NaCl KCl CuCl2 | |
| D. | Fe2(SO4)3 K2CO3 KHSO4 NH4Cl |
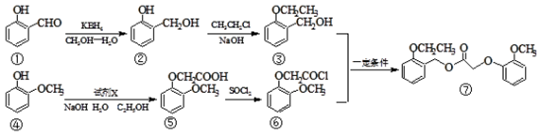
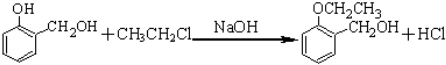 .
.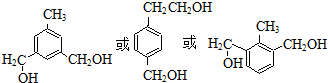 (写出一种
(写出一种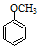 +HBr→
+HBr→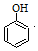 +CH3Br
+CH3Br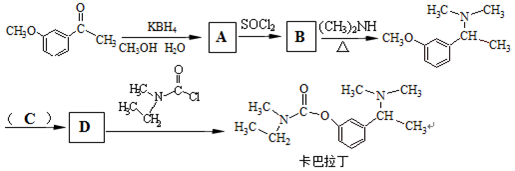
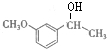 B:
B: C:HBrD:
C:HBrD: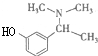 .
.