题目内容
用惰性电极电解某溶液时,发现两极只有H2和O2生成,则电解一段时间后,若电解前后温度变化忽略不计,下列有关溶液叙述正确的有( )
①该溶液的pH可能增大
②该溶液的pH可能减小
③该溶液的pH可能不变
④该溶液的浓度可能增大
⑤该溶液的浓度可能不变
⑥该溶液的浓度可能减小.
①该溶液的pH可能增大
②该溶液的pH可能减小
③该溶液的pH可能不变
④该溶液的浓度可能增大
⑤该溶液的浓度可能不变
⑥该溶液的浓度可能减小.
| A、①②③④⑤ |
| B、只有①②③④ |
| C、只有①③⑤ |
| D、①②③④⑤⑥ |
考点:电解原理
专题:
分析:用惰性电极电解某溶液时,发现两极只有H2和O2生成,实质上是电解水型装置,电解时溶液中的溶质为强碱、含氧的强酸或强酸强碱盐,根据溶液中溶质浓度、酸碱性分析解答.
解答:
解:用惰性电极电解某溶液时,发现两极只有H2和O2生成,实质上是电解水型装置,电解时溶液中的溶质为强碱、含氧的强酸或强酸强碱盐,
电解强碱溶液时,实质上是电解水,溶液的体积减小,溶质的物质的量不变,则溶液浓度增大,溶液的pH增大;
电解含氧强酸时,实质上是电解水,溶液体积减小,溶质的物质的量不变,则酸浓度增大,溶液的pH减小;
电解强酸强碱盐时,实质上是电解水,溶液体积减小,溶质的物质的量不变,溶液的浓度增大,但溶质不水解,溶液仍然是强酸强碱盐溶液,溶液呈中性,pH不变,
通过以上分析知,电解过程中溶液的pH可能增大、减小或不变,但溶液浓度增大,
故选B.
电解强碱溶液时,实质上是电解水,溶液的体积减小,溶质的物质的量不变,则溶液浓度增大,溶液的pH增大;
电解含氧强酸时,实质上是电解水,溶液体积减小,溶质的物质的量不变,则酸浓度增大,溶液的pH减小;
电解强酸强碱盐时,实质上是电解水,溶液体积减小,溶质的物质的量不变,溶液的浓度增大,但溶质不水解,溶液仍然是强酸强碱盐溶液,溶液呈中性,pH不变,
通过以上分析知,电解过程中溶液的pH可能增大、减小或不变,但溶液浓度增大,
故选B.
点评:本题考查电解原理,明确离子放电顺序是解本题关键,知道电解实质即可解答,电解池有电解水型、电解电解质型、放氢生碱型、放氧生酸型,根据溶质的特点确定电解类型,从而确定电解后溶液酸碱性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
温度为T时,向4.0L恒容密闭容器中充入2.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0064 mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11 mol?L-1,则反应的△H<0 |
| C、相同温度下,起始时向容器中充入4.0molPCl3、4.0molCl2,达到平衡时,PCl3的转化率等于80% |
| D、相同温度下,起始时向容器中充入2.0molPCl5、0.40molPCl3和0.40molCl2,达到平衡前v(正)<v(逆) |
在水溶液中能大量共存的一组离子是( )
| A、NH4+、Na+、Cl-、SO42- |
| B、K+、Mg2+、OH-、NO3- |
| C、H+、Ca2+、SiO32-、NO3- |
| D、K+、Al3+、ClO-、HCO3- |
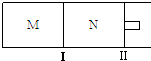 如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中都通入xmolA和ymolB的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g)+3B(g)?2C(g)△H=-192kJ?mol-1.向M、N中都通入xmolA和ymolB的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )| A、若平衡时A气体在两容器中的体积分数相等,则x一定等于y |
| B、若x:y=1:2,则平衡时,M中的转化率:A>B |
| C、若x:y=1:3,当M中放出热量172.8 kJ时,A的转化率为90% |
| D、若x=1.2,y=1,N中达到平衡时体积为2 L,含有0.4mol C,再通入0.36 mol A时,v(逆)>v(正) |
向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,充分反应后发现有少量金属析出,过滤后往滤液中滴加稀盐酸,有白色沉淀生成,则析出的少量金属为( )
| A、Fe和Cu | B、Ag |
| C、Fe和Ag | D、Ag和Cu |