题目内容
4.如表为元素周期表中的一部分,表中列出10种元素在周期表中的位置,按要求回答下列问题.族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素①的单质在氧气中燃烧,生成的氧化物的化学式是CO2.
(3)第3周期主族元素中,元素原子半径最小的是Cl(填元素符号).
(4)元素⑨的单质和石灰乳作用可制取漂白粉,该反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(5)元素④的原子最外层电子数为7.
(6)元素⑦的氧化物常用于制造光导纤维(填一种高性能的现代通讯材料的名称).
(7)元素⑧、⑨中,化学性质较不活泼的元素是S(填元素符号),氢化物较稳定的是HCl(填化学式).
(8)元素②的氢化物化学式NH3,元素⑨的最高价氧化物的水化物的化学式HClO4
(9)元素⑤的氢氧化物和稀盐酸反应的化学方程式NaOH+HCl=NaCl+H2O.
分析 由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Si、⑧为S、⑨为Cl、⑩为Ar.
(1)稀有气体原子最外层为稳定结构,化学性质最不活泼;
(2)碳在氧气中燃烧生成二氧化碳;
(3)同周期自左而右原子半径减小;
(4)氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水;
(5)主族元素原子最外层电子数等于族序数;
(6)元素⑦的氧化物为二氧化硅,常用于制造光导纤维;
(7)同周期自左而右金属性减弱,非金属性越强,氢化物越稳定;
(8)元素②的氢化物为氨气,元素⑨的最高价氧化物的水化物为高氯酸;
(9)氢氧化钠与盐酸反应生成氯化钠与水.
解答 解:由元素在周期表中位置,可知①为C、②为N、③为O、④为F、⑤为Na、⑥为Mg、⑦为Si、⑧为S、⑨为Cl、⑩为Ar.
(1)稀有气体Ar的原子最外层为稳定结构,化学性质最不活泼,故答案为:氩;
(2)碳在氧气中燃烧生成CO2,故答案为:CO2;
(3)同周期自左而右原子半径减小,第三周期主族元素中Cl原子半径最小,故答案为:Cl;
(4)氯气与氢氧化钙反应生成氯化钙、次氯酸钙与水,反应方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(5)元素④处于第VIIA族,原子最外层电子数为7,故答案为:7;
(6)元素⑦的氧化物为二氧化硅,常用于制造光导纤维,故答案为:光导纤维;
(7)同周期自左而右金属性减弱,则非金属性S<cl,故S的活泼性较弱,非金属性越强,氢化物越稳定,故HCl更稳定,故答案为:S;HCl;
(8)元素②的氢化物为NH3,元素⑨的最高价氧化物的水化物为HClO4,故答案为:NH3;HClO4;
(9)氢氧化钠与盐酸反应生成氯化钠与水,反应方程式为:NaOH+HCl=NaCl+H2O,故答案为:NaOH+HCl=NaCl+H2O.
点评 本题考查元素周期表与元素周期律,难度不大,注意整体把握元素周期表的结构,理解掌握元素周期律.

 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案| A. | 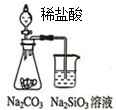 如图可能证明非金属性强弱:Cl>C>Si | |
| B. | 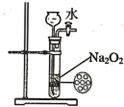 如图装置可用来制备少量氧气,并且控制反应的发生与停止 | |
| C. | 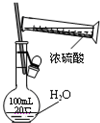 图中配制一定物质的量浓度的硫酸溶液不能直接在容量瓶中进行 | |
| D. | 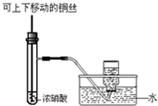 如图为制备并收集少量NO2气体 |
| A. | .甲溶液含有OH- | B. | .乙溶液含有H+ | C. | 丙溶液含有HCO3- | D. | .丁溶液含有NH4+ |
| A. | 6.8g液态KHSO4中含有0.1NA个阳离子 | |
| B. | NA个Fe(OH)3胶体粒子形成的纳米材料的质量为107g | |
| C. | 等体积等密度的N2和CO所含分子数相同 | |
| D. | 含NA个Na+的Na2O溶解于水1L水中,Na+的物质的量浓度为1mol•L-1 |
| A. | 1.0mol | B. | 1.6mol | C. | 2.2mol | D. | 2.4mol |
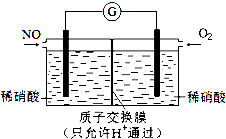 NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
NO和NO2是常见的氮氧化物,研究它们的综合利用有重要意义.
 如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: