题目内容
A-F有如图所示的转化关系(反应条件未标出),已知反应①是置换反应.请回答下列问题:

(1)若B是黄绿色气体,C、F是空气的主要成分,A、D相遇有白烟生成.
①写出A的电子式 .
②写出反应①中直接产生白烟的化学方程式为 .
③有同学模仿排饱和食盐水收集氯气的方法,想用排饱和白烟的水溶液的方法收集A气体.你认为能否达到目的? (填“能”或“否”),理由是.
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,则写出反应①的化学方程式为 ;说出B的一个重要用途 .
(3)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行.若C的溶液在空气中暴露一定时间后,要证明该溶液中的阳离子未被氧化完的实验方法是 .

(1)若B是黄绿色气体,C、F是空气的主要成分,A、D相遇有白烟生成.
①写出A的电子式
②写出反应①中直接产生白烟的化学方程式为
③有同学模仿排饱和食盐水收集氯气的方法,想用排饱和白烟的水溶液的方法收集A气体.你认为能否达到目的?
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,则写出反应①的化学方程式为
(3)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行.若C的溶液在空气中暴露一定时间后,要证明该溶液中的阳离子未被氧化完的实验方法是
考点:无机物的推断
专题:推断题
分析:(1)若B是黄绿色气体应为Cl2,C、F是空气的主要成分,结合转化关系F为O2,由于氧的氧化性较氯气稍强,故氯气置换出的应该是氮气,C为N2,C+F→E,为N2+O2
2NO;A、D相遇有白烟生成,判断A为NH3,D为HCl;
(2)反应①是置换反应,而且涉及的单质都是非金属,所以可以考虑氧族里氧气置换出硫的反应,卤素单质之间的置换(氧化性较强的单质置换出氧化性较弱的单质);碳族里碳置换出硅的反应.再结合与F的反应可以推断出B应该是二氧化硅,原子晶体;
(3)金属置换出气体很容易就想到活泼金属置换出氢气,再结合能与F连续反应,可以推断出是铁和盐酸的反应;反应②的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-.
| ||
(2)反应①是置换反应,而且涉及的单质都是非金属,所以可以考虑氧族里氧气置换出硫的反应,卤素单质之间的置换(氧化性较强的单质置换出氧化性较弱的单质);碳族里碳置换出硅的反应.再结合与F的反应可以推断出B应该是二氧化硅,原子晶体;
(3)金属置换出气体很容易就想到活泼金属置换出氢气,再结合能与F连续反应,可以推断出是铁和盐酸的反应;反应②的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-.
解答:
解:(1)若B是黄绿色气体应为Cl2,C、F是空气的主要成分,结合转化关系F为O2,由于氧的氧化性较氯气稍强,故氯气置换出的应该是氮气,C为N2,C+F→E,为N2+O2
2NO;A、D相遇有白烟生成,判断A为NH3,D为HCl,
①A为NH3,电子式为 ,故答案为:
,故答案为: ;
;
②A、D相遇有白烟生成,所以发生反应为NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
③因氨气极易溶于水,饱和氯化铵对氨气的溶解度不大,不能用排饱和氯化铵溶液的方法收集氨气,故答案为:否;氯化铵对氨气在水中的溶解度影响不大;
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,反应A+B→C+D是非金属间的置换反应,可以分析第ⅣA、ⅥA、ⅤⅡA 主族元素单质间的置换反应,结合转化关系中 F的反应,只有2C+SiO2
Si+2CO 符合,所以A为C,B为 SiO2,二氧化硅属于原子晶体,主要用途为:制光导纤维,石英钟表,石英玻璃,晶体硅,电脑芯片等,
故答案为:2C+SiO2
Si+2CO;制光导纤维,石英钟表,石英玻璃,晶体硅,电脑芯片等;
(3)金属置换出气体很容易就想到活泼金属置换出氢气,再结合能与F连续反应,可以推断出是铁和盐酸的反应;反应②的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,A为Fe,B为HCl,C为FeCl2,D为H2,E为FeCl3,F为Cl2,如FeCl2溶液中的阳离子未被氧化完,则应存在Fe2+,可用酸性高锰酸钾检验,取该C的水溶液少许,滴加2-3滴酸性高锰酸钾溶液,若紫色褪去,说明该溶液中的亚铁例子还未被氧化完,反之则已被氧化完,
故答案为:取该C的水溶液少许,滴加2-3滴酸性高锰酸钾溶液,若紫色褪去,说明该溶液中的亚铁例子还未被氧化完,反之则已被氧化完.
| ||
①A为NH3,电子式为
 ,故答案为:
,故答案为: ;
;②A、D相遇有白烟生成,所以发生反应为NH3+HCl=NH4Cl,故答案为:NH3+HCl=NH4Cl;
③因氨气极易溶于水,饱和氯化铵对氨气的溶解度不大,不能用排饱和氯化铵溶液的方法收集氨气,故答案为:否;氯化铵对氨气在水中的溶解度影响不大;
(2)若A、D、F都是非金属单质,A、D所含元素同主族,A、F所含元素同周期,反应A+B→C+D是非金属间的置换反应,可以分析第ⅣA、ⅥA、ⅤⅡA 主族元素单质间的置换反应,结合转化关系中 F的反应,只有2C+SiO2
| ||
故答案为:2C+SiO2
| ||
(3)金属置换出气体很容易就想到活泼金属置换出氢气,再结合能与F连续反应,可以推断出是铁和盐酸的反应;反应②的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,A为Fe,B为HCl,C为FeCl2,D为H2,E为FeCl3,F为Cl2,如FeCl2溶液中的阳离子未被氧化完,则应存在Fe2+,可用酸性高锰酸钾检验,取该C的水溶液少许,滴加2-3滴酸性高锰酸钾溶液,若紫色褪去,说明该溶液中的亚铁例子还未被氧化完,反之则已被氧化完,
故答案为:取该C的水溶液少许,滴加2-3滴酸性高锰酸钾溶液,若紫色褪去,说明该溶液中的亚铁例子还未被氧化完,反之则已被氧化完.
点评:本题考查元素化合物的推断,属于拼合型题目,题目信息量大,难度较大,需要学生熟练掌握常见元素化合物的性质,侧重考查学生分析解决问题的能力.

练习册系列答案
相关题目
下列关于蛋白质的说法不正确的是( )
| A、重金属盐能使蛋白质变性,所以误食重金属盐时,可以喝牛奶解毒 |
| B、阿胶的主要成分是蛋白质,蚕丝的主要成份是纤维素 |
| C、蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,再加水,重新溶解 |
| D、浓硝酸溅到皮肤上,会使皮肤呈现黄色 |
把200mL NH4HCO3和Na2CO3的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全.该混合溶液中c(Na+)为( )
| A、(l0b-5a))mol/L | ||||
| B、(2b-a)mol/L | ||||
C、(
| ||||
D、(5b-
|
几种短周期元素的原子半径及主要化合价如表:下列叙述错误的是( )
| 元素代号 | L | M | X | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A、R的氧化物对应的水化物可能具有两性 |
| B、X单质在氧气中燃烧不可能生成XO3 |
| C、离子半径大小:r(M3+)>r(T2-) |
| D、L2+和X2-的核外电子数相等 |

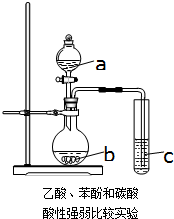 化学研究性学习小组进行验证乙酸、碳酸和苯酚溶液的酸性强弱的探究实验.设计如图一次性完成乙酸、碳酸和苯酚溶液酸性强弱验证的实验装置.
化学研究性学习小组进行验证乙酸、碳酸和苯酚溶液的酸性强弱的探究实验.设计如图一次性完成乙酸、碳酸和苯酚溶液酸性强弱验证的实验装置.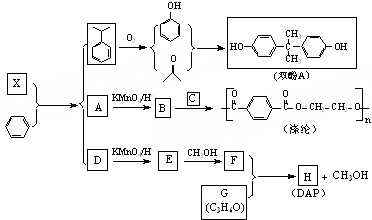
 Na、Cu、Al、O、C、H是常见的六种元素.
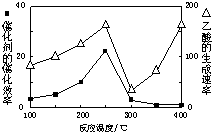
Na、Cu、Al、O、C、H是常见的六种元素.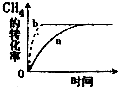 碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.
碳及其化合物在人类生产、生活中的应用非常广泛.“低碳生活”不再只是一种理想,更是一种值得期待的生活方式.