题目内容
下列说法错误的是( )
| A、对羟基苯甲酸的沸点比邻羟基苯甲酸高,冰中既存在范德华力,又存在氢键 |
| B、简单立方是非密置层三维堆积形成的,面心立方是由密置层三维堆积形成的 |
| C、所有共价键都有方向性,形成氢键的三个相关原子可以不在直线上 |
| D、金属晶体的导电、导热性都与自由电子有关,离子晶体在一定条件下可以导电 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A、对羟基苯甲酸存在分子间氢键,邻羟基苯甲酸存在分子内氢键;冰中既存在范德华力,又存在氢键;
B、根据简单立方与面心立方的堆积方式分析;
C、s轨道为球形,s-s σ键没有方向性;
D、金属晶体中的自由电子定向移动为电流,自由电子的移动能传递热能,熔融状态时离子晶体能电离.
B、根据简单立方与面心立方的堆积方式分析;
C、s轨道为球形,s-s σ键没有方向性;
D、金属晶体中的自由电子定向移动为电流,自由电子的移动能传递热能,熔融状态时离子晶体能电离.
解答:
解:A、对羟基苯甲酸存在分子间氢键,邻羟基苯甲酸存在分子内氢键,所以对羟基苯甲酸的沸点比邻羟基苯甲酸高;冰中既存在范德华力,又存在氢键,故A正确;
B、简单立方堆积是将非密置层一层一层地在三维空间里堆积,面心立方的堆积是由密置层在三维空间里堆积形成,故B正确;
C、s轨道为球形,s-s σ键没有方向性,形成氢键的三个相关原子可以不在直线上,故C错误;
D、给金属晶体加电压时,晶体中的自由电子定向移动形成电流,自由电子的移动能传递热能,熔融状态时离子晶体能电离,所以能导电,故D正确;
故选C.
B、简单立方堆积是将非密置层一层一层地在三维空间里堆积,面心立方的堆积是由密置层在三维空间里堆积形成,故B正确;
C、s轨道为球形,s-s σ键没有方向性,形成氢键的三个相关原子可以不在直线上,故C错误;
D、给金属晶体加电压时,晶体中的自由电子定向移动形成电流,自由电子的移动能传递热能,熔融状态时离子晶体能电离,所以能导电,故D正确;
故选C.
点评:本题考查了氢键、晶体的堆积方式、共价键的方向性、金属晶体的性质等,题目涉及的知识点较多,侧重于基础知识的考查,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法不正确的是( )
| A、葡萄糖不可能由纤维素制取 |
| B、葡萄糖在酒化酶作用下转化为乙醇和二氧化碳 |
| C、葡萄糖是人体能量的重要来源 |
| D、葡萄糖能与银氨溶液发生反应 |
设NA表示阿佛加德罗常数,下列说法正确的是( )
| A、33.6L(常温常压)氯气与2.7g铝充分反应,转移电子数为0.3NA |
| B、在标准状况下,22.4L CH2Cl2中含有的氢原子数为2NA |
| C、标准状况下,22.4L己烷含有的共价键数目为19NA |
| D、46gNO2气体在标准状况下的体积为22.4L |
下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合生成稳定化合物的是( )
| A、6与16 | B、8与14 |
| C、10与19 | D、11与17 |
由乙烯的结构和性质推测丙烯(CH2═CH-CH3)的结构或性质正确的是( )
| A、不能使酸性高锰酸钾溶液褪色 |
| B、不能在空气中燃烧 |
| C、能使溴的四氯化碳溶液褪色 |
| D、与HCl在一定条件下能加成并只得到一种产物 |
下列关于苯酚的叙述不正确的是( )
| A、苯酚是一种弱酸,滴加指示剂变色 |
B、苯酚在水溶液中能按下式电离: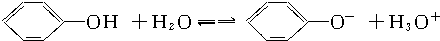 |
| C、苯酚钠在水溶液中几乎不能存在,会水解生成苯酚,所以苯酚钠溶液显碱性 |
| D、苯酚有腐蚀性,溅在皮肤上可用酒精冲洗 |
卤族元素有F、Cl、Br、I、At等元素,下列关于At的推断不正确的是( )
| A、At2的颜色比I2深 |
| B、HAt的水溶液的酸性比盐酸强 |
| C、AgAt不溶于水 |
| D、HAt很稳定,受热不易分解 |
