题目内容
12.在含2.408×1024个Na+的Na2SO4的物质的量是( )| A. | 0.1mol | B. | 0.5 mol | C. | 1 mol | D. | 2 mol |
分析 结合n=$\frac{N}{{N}_{A}}$及物质构成计算.
解答 解:n(Na+)=$\frac{2.408×1{0}^{24}}{6.02×1{0}^{23}}$=4mol,则n(Na2SO4)=$\frac{4mol}{2}$=2mol,
故选D.
点评 本题考查物质的量的计算,为高频考点,把握物质的构成、物质的量与微粒数的关系为解答的关键,侧重分析与计算能力的考查,注意基本计算公式的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列热化学方程式或离子方程式中,正确的是( )
| A. | 甲烷的标准燃烧热为890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) $?_{500℃、30MPa}^{催化剂}$ 2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 氯化镁溶液与氨水反应:Mg2++2NH3•H2O═Mg(OH)2↓+2NH4+ | |
| D. | 氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O═2Al(OH)3 |
16.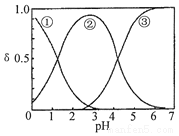 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
 H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )
H2C2O4水溶液中H2C2O4、HC2O4-和C2O42-三种形态的粒子的分布分数δ随溶液pH变化的关系如图所示,下列说法正确的是( )| A. | 曲线①代表的粒子是HC2O4- | |
| B. | 0.1mol•L-1NaHC2O4溶液中:c(C2O42-)>c(H2C2O4) | |
| C. | pH=5时,溶液中主要含碳微粒浓度大小关系为:c(C2O42-)>c(H2C2O4)>c(HC2O4-) | |
| D. | 在一定温度下,往CaC2O4饱和溶液中加入少量CaCl2固体,c(C2O42-)将减小,c(Ca2+)增大 |
13.利用如图所示装置进行下列实验,装置正确并能达到实验目的是( )
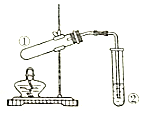

| 选项 | ①中试剂 | ②中溶液 | 实验目的 |
| A | 二氧化锰(s),浓盐酸 | 饱和食盐水 | 制取氯气 |
| B | Na2SO3(s),70%H2SO4 | 酸性高锰酸钾 | 验证SO2的还原性 |
| C | Na2CO3(s)或NaHCO3(s) | 澄清石灰水 | 鉴别Na2CO3和NaHCO3 |
| D | 乙醇、乙酸、浓硫酸 | 饱和碳酸钠 | 制取乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
7.下列溶液氯离子的物质的量浓度与50mL 1mol•L-1AlCl3溶液中氯离子的物质的量浓度相等的是( )
| A. | 150 mL 1 mol•L-1氯化钠溶液 | B. | 75 mL 3 mol•L-1氯化钙溶液 | ||
| C. | 150 mL 3 mol•L-1氯化钾溶液 | D. | 50 mL 3 mol•L-1氯化镁溶液 |
17.下列离子方程式正确的是( )
| A. | 向NH4HSO3溶液中,加入过量的氢氧化钠溶液,并加热:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 向FeBr2溶液中通入过量氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | FeCl3溶液与Cu的反应:Cu+2Fe3+=Cu2++2Fe2+ | |
| D. | 向次氯酸钠溶液中通入少量SO2气体:2ClO-+SO2+H2O=2HClO+SO32- |
4.下列说法错误的是( )
| A. | 焰色反应与电子跃迁有关 | |
| B. | P4和CH4都是正四面体分子且键角都为109°28′ | |
| C. | 元素电负性越大的原子,吸引电子的能力越强 | |
| D. | 根据对角线规则,H3BO3是弱酸 |
1.下列溶液中,跟100mL 1mol/L NaCl溶液所含的Cl-数目相同的是( )
| A. | 25mL 0.5mol/L HCl溶液 | B. | 200mL 0.5mol/L KCl溶液 | ||
| C. | 50mL 1mol/L NaCl溶液 | D. | 100mL 0.5mol/L MgCl2溶液 |
2.下列说法正确的是( )
| A. | 32gO2占有的体积为 22.4L | |
| B. | 22.4LN2 含有阿伏加德罗常数个 N2 | |
| C. | 在标准状况下,22.4L 水的物质的量为 1mol | |
| D. | 22gCO2 和 16gO2,在同温、同压下占有的体积相同 |