题目内容
7.某化学兴趣小组为探究铜跟浓硫酸反应,用如图装置进行有关实验.请回答下列问题: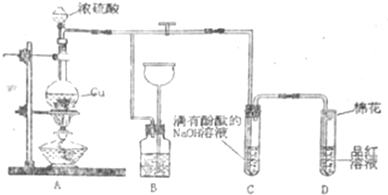
(1)装置A中发生的化学反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是④(填序号);
①水 ②酸性KMnO4 ③Na2CO3溶液 ④饱和的NaHSO3溶液
(3)装置C和D中产生的现象相同,但原因却不同.C中是由于SO2溶液具有酸性中和了溶液中的NaOH,而D中则是由于SO2具有漂白性;
(4)装置D中试管口塞一团棉花,棉花中应浸有一种液体,其作用是吸收多余的二氧化硫,防止污染空气;
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色,为了证明蓝色只与Cu2+有关,而与其它离子无关,某同学设计了下列实验,其中对实验目的没有意义的是②③(填序号);
①观察稀H2SO4溶液呈无色
②观察CuSO4粉末呈白色
③稀释CuSO4溶液,溶液蓝色变浅
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍显蓝色
(6)若实验中用7.2g铜片和12.5ml18.0ml•L-1的浓硫酸在加热条件充分反应,最终铜片仍有剩余.根据所学的知识,某同学认为溶液中一定还有硫酸剩余,其理由是反应过程中浓H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应.
假定反应前后溶液的体积不变,设剩余硫酸的浓度为amol/L,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾$\frac{a}{240}$mol(用含a的代数式表示,要化简).
分析 浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,反应生成的SO2具有酸性和还原性,可用排饱和NaHSO3溶液收集,具有漂白性,可使品红溶液褪色,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,结合题目要求解答该题,
(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应生成硫酸铜、二氧化硫和水;
(2)SO2易溶于水,具有酸性和还原性;
(3)SO2溶液具有酸性,可与NaOH溶液反应,具有漂白性,可使品红溶液褪色;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓硫酸与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,依据氧化还原反应单质转移守恒计算得到.
解答 解:(1)浓硫酸具有强氧化性,在加热条件下与铜发生氧化还原反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)SO2易溶于水,具有酸性和还原性,可与酸性KMnO4、Na2SO3溶液反应,难溶于水饱和的NaHSO3溶液,可用排饱和NaHSO3溶液收集,
故答案为:④;
(3)SO2溶液具有酸性,可与NaOH溶液反应,发生:SO2+2OH-=SO32-+H2O,则滴加酚酞的氢氧化钠溶液褪色,具有漂白性,可使品红溶液褪色,
故答案为:溶液具有酸性,中和了溶液中的NaOH;漂白性;
(4)二氧化硫有毒,不能排放到空气中,应可氢氧化钠溶液反应,则棉花上可浸有氢氧化钠溶液,防止污染空气,
故答案为:吸收多余的二氧化硫,防止污染空气;
(5)①观察稀硫酸溶液呈无色,可说明SO42-无色;
②观察CuSO4粉末呈白色,不能证明蓝色只与Cu2+有关;
③稀释CuSO4溶液,溶液蓝色变浅,因阳离子和阴离子浓度都变浅,不能证明;
④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色,铜离子浓度减小,可说明与铜离子有关;
⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色,铜离子物质的量不变,可说明与铜离子有关,
则对实验目的没有意义的是②③,
故答案为:②③;
(6)浓硫酸具有强氧化性,而稀硫酸与铜不反应,随着反应的进行,硫酸浓度不断降低,稀硫酸与铜不反应,则反应后溶液中一定含有硫酸,浓H2SO4与铜反应的过程中,浓度会变稀,而稀硫酸不与铜反应,所以会有剩余,加入硝酸钾后,硝酸根离子在氢离子存在情况下有强氧化性,能与铜反应,剩余硫酸浓度为amol/L,则硫酸物质的量=0.0125L×amol/L=0.0125amol,n(Cu)=$\frac{7.2g}{64g/mol}$=0.1125mol,n(H2SO4)=0.0125L×18mol/L=0.225mol,参加反应的硫酸物质的量=0.225mol-0.0125amol,Cu+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,2mol硫酸反应单质转移2mol,则电子转移为:0.225mol-0.0125amol,设加入硝酸钾物质的量为x,依据电子守恒列式计算得到:0.1125mol×2=0.225mol-0.0125amol+3x,得到x=$\frac{a}{240}$mol,
故答案为:反应过程中浓H2SO4被不断消耗,生成的水逐渐增多,使浓硫酸逐渐变稀,至一定浓度就不再与铜片反应;$\frac{a}{240}$;
点评 本题综合考查性实验设计、电子转移守恒的计算,侧重于学生的分析能力和实验能力的考查,为高考常见题型,题目难度中等,注意把握相关物质的性质以及实验原理.

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案| A. | 950mL,111.2g | B. | 500mL,117g | C. | 1000mL,l17g | D. | 任意规格,117g |
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)②、⑧、⑦的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2CO3>H2SiO3 .
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的电子式:
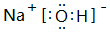 .
.(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为(填序号)ab.
a.MnO2 b.FeCl3c.Na2SO3d.KMnO4
(5)由①和②两种元素组成的某种物质是天然气的主要成分,该物质4g完全燃烧生成CO2气体和液态水时放出222.5kJ的热量,则该物质燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890kJ/mol
(6)把②和⑥的条状单质用导线相连,放在由①④⑤三种元素组成的化合物的水溶液中,该装置可实现由化学能转化为电能,在该装置中单质⑥做负极,该电极反应式为Al-3e-+4 OH-=AlO2-+2H2O.
| A. | 稀醋酸与氢氧化钠溶液的反应:H++OH-=H2O | |
| B. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| C. | 氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=2Cl-+2Fe3+ | |
| D. | 碳酸钙溶液与足量稀盐酸的反应:CO32-+2H+=H2O+CO2↑ |
| A. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| B. | PM2.5(2.5微米以下的细颗粒物)主要来自化石燃料的燃烧 | |
| C. | 处理废水时加入明矾作为消毒剂对水进行杀菌消毒 | |
| D. | 某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |