题目内容
下列化学用语书写正确的是( )
A、甲烷的电子式: |
| B、乙醛的结构简式:CH3COH |
| C、乙烯的结构式:CH2=CH2 |
D、乙醇的结构式: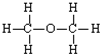 |
考点:电子式,结构式,结构简式
专题:化学用语专题
分析:A、甲烷中碳原子与四个氢原子形成四个共价键;
B、醛基的结构简式:-CHO;
C、结构式是利用短线表示共价键;
D、乙醇中含有CH3CH2-和-OH.
B、醛基的结构简式:-CHO;
C、结构式是利用短线表示共价键;
D、乙醇中含有CH3CH2-和-OH.
解答:
解:A、甲烷中碳原子与四个氢原子形成四对共用电子对,故A正确;
B、在醛基中,碳原子与氧原子形成双键,与氢原子形成单键,醛基的结构简式:-CHO,故B错误;
C、结构式是利用短线表示共价键,CH2=CH2属于结构简式,故C错误;
D、乙醇中含有CH3CH2-和-OH,结构式为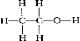 ,故D错误.
,故D错误.
故选A.
B、在醛基中,碳原子与氧原子形成双键,与氢原子形成单键,醛基的结构简式:-CHO,故B错误;
C、结构式是利用短线表示共价键,CH2=CH2属于结构简式,故C错误;
D、乙醇中含有CH3CH2-和-OH,结构式为
 ,故D错误.
,故D错误.故选A.
点评:本题考查电子式、结构简式、键线式等,难度不大,注意键线式是进一步省去碳氢元素的符号,只要求表示出碳碳键以及与碳原子相连的基团,键线式中每个拐点和终点均表示一个碳原子,每个碳原子都形成四个共价键,不足的用氢原子补足.

练习册系列答案
相关题目
下面不是化学方法处理污水的是( )
| A、过滤法 | B、混凝法 |
| C、中和法 | D、沉淀法 |
下列反应的离子反应方程式书写正确的是( )
| A、少量金属钠加到冷水中:Na+H2O=Na++OH-+H2↑ |
| B、铁与稀盐酸反应:2Fe+6H+=2 Fe3++3H2↑ |
| C、氯气通入冷的氢氧化钠溶液中:Cl2+2OH-=Cl-+ClO-+H2O |
| D、过量的二氧化碳通入氢氧化钠溶液:CO2+2OH-=CO32-+H2O |
下列说法中不正确的是( )
| A、蓄电池在放电过程中,负极质量增加,正极质量也增加 |
| B、电解法是最强有力的氧化还原手段,可以将极难还原的活泼金属从它们的化合物中还原出来 |
| C、钢铁发生吸氧腐蚀时,负极反应式为:Fe-3e-═Fe3+ |
| D、电解精炼铜时,用纯铜板作阴极,粗作阳极,用硫酸铜溶液作电解液铜板 |
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g)△H=-221kJ?mol-1 ②稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1,下列结论正确的是( )
| A、反应①为放热反应 |
| B、碳的燃烧热大于110.5 kJ?mol-1 |
| C、浓硫酸和NaOH反应的中和热为-57.3 kJ?mol-1 |
| D、稀醋酸与稀NaOH反应生成1mol水,放出57.3 kJ的热量 |
设NA为阿伏加德罗常数的数值,下列叙述中正确的是( )
| A、标准状况下,22.4L氯气与足量的NaOH溶液反应,转移的电子数目为2NA |
| B、1L 0.5mol/L FeCl3溶液中Fe3+数目为0.5NA |
| C、常温常压下,8.8g丙烷中所含电子数为5.2NA |
| D、78g过氧化钠中所含阴离子数目为2NA |
下列反应中原子利用率达100%的是( )
A、制聚乙烯:nCH2═CH2?
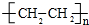 ? ? | ||||
B、制CuSO4:Cu+2H2SO4(浓)
| ||||
C、 | ||||
D、制乙烯:C4H10
|
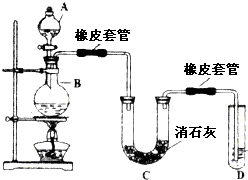 瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色、刺激性气味的气体--氯气.某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(该反应是放热反应),据此回答下列问题:
瑞典化学家舍勒在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色、刺激性气味的气体--氯气.某学生使用这一原理设计如图所示的实验装置,并且利用制得的氯气与潮湿的消石灰反应制取少量漂白粉(该反应是放热反应),据此回答下列问题: