题目内容
1.分析下列反应在任何温度下均能自发进行的是( )| A. | 2N2(g)+O2(g)═2N2O(g)△H=+163 kJ•mol-1 | |
| B. | Ag(s)+$\frac{1}{2}$Cl2(g)═AgCl(s)△H=-127 kJ•mol-1 | |
| C. | HgO(s)═Hg(l)+$\frac{1}{2}$O2(g)△H=+91 kJ•mol-1 | |
| D. | H2O2(l)═$\frac{1}{2}$O2(g)+H2O(l)△H=-98 kJ•mol-1 |
分析 △H-T△S<0的反应可自发进行,结合焓变、熵变判断.
解答 解:A.△H>0、△S<0,则△H-T△S>0,该反应在任何温度不能自发进行,故A不选;
B.△H<0、△S<0,该反应在高温下不能自发进行,故B不选;
C.△H>0、△S>0,该反应在低温下不能自发进行,故C不选;
D.△H<0、△S>0,则△H-T△S<0,该反应在任何温度均能自发进行,故D选;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握焓变、熵变对反应进行方向的影响为解答的关键,侧重分析与应用能力的考查,注意综合判据的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.以锌锰废电池中的碳包为原料回收MnO2的过程中涉及如下反应:
①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1
③2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H3
则下列判断正确的是( )
①MnO2(s)+C(s)═MnO(s)+CO(g)△H1=+24.4kJ•mol-1
②MnO2(s)+CO(g)═MnO(s)+CO2(g)△H2=-148.1kJ•mol-1
③2MnO2(s)+C(s)═2MnO(s)+CO2(g)△H3
则下列判断正确的是( )
| A. | 碱性锌锰干电池属于二次电池 | B. | △H3=△H1+△H2 | ||
| C. | 反应①的活化能为24.4 kJ•mol-1 | D. | △H1<△H3 |
10.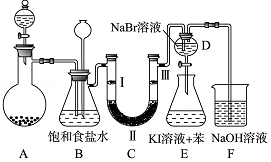 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象长颈漏斗中发生倒吸,液面上升.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,溶液中发生的反应方程式为Cl2+2NaBr=Br2+2NaCl;打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象溶液分层,上层为紫色溶液,下层为无色液体.说明氯、溴、碘单质的氧化性强弱顺序为Cl2>Br2>I2.
 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象长颈漏斗中发生倒吸,液面上升.
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入D
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |