题目内容
18.液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨在燃烧实验中相关的反应有:①4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1
②4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2
③4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1=$\frac{3△{H}_{2}+2△{H}_{3}}{5}$.
分析 由反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1 ①
4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2 ②
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3③
则反应$\frac{②×3+③×2}{5}$可得到反应①,据此进行分析.
解答 解:由反应4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1 ①
4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2 ②
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3③
则反应$\frac{②×3+③×2}{5}$可得到反应①,则△H1=$\frac{3△{H}_{2}+2△{H}_{3}}{5}$,
故答案为△H1=$\frac{3△{H}_{2}+2△{H}_{3}}{5}$.
点评 本题考查了盖斯定律的应用,注意方程式①②与③中化学计量数的关系是本题解题的关键,题目难度中等.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
7.为了美化南实校园,让学生有一个更清幽的学习环境,学校建成了校园樱花大道,还移栽了许多的桂花树,为了使移栽的树很好地适应新的土壤环境并提高其成活率,每株树上都给挂上了大树营养液,这种营养液的主要成分是已酸二乙氨基乙醇酯,又名:DA-6,其结构简式:CH3(CH2)4COOCH2CH2N(C2H5)2下列有关说法正确的是( )
| A. | 该化合物的含氧官能团为羰基和醚键 | |
| B. | 该化合物的红外光谱有7种振动吸收 | |
| C. | 该化合物的核磁共振氢谱有9组峰 | |
| D. | 该有机物能与水混溶 |
6.已知X、Y元素同周期,且电负性X<Y,下列说法错误的是( )
| A. | 第一电离能X可能大于Y | |
| B. | 气态氢化物的稳定性:HmY小于HmX | |
| C. | 最高价含氧酸的酸性:X对应的酸性弱于Y对应的酸性 | |
| D. | X和Y形成化合物时,X显正价,Y显负价 |
3.下列分离混合物常见的仪器:从左至右,用于分离操作正确的是( )
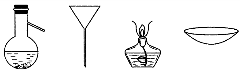

| A. | 蒸发、萃取、蒸馏、过滤 | B. | 蒸馏、过滤、蒸发、蒸发 | ||
| C. | 萃取、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、萃取、蒸馏 |
10.下列说法正确的是( )
| A. | 若电解熔融MgCl2产生1 mol Mg,理论上转移的电子数约为2×6.02×1023 | |
| B. | 常温下,C(s)+H2O(g)?CO(g)+H2(g) 不能自发进行,则该反应的△H>0 | |
| C. | 石墨能导电,所以石墨属于电解质 | |
| D. | 一定条件下反应2SO2+O2?2SO3达到平衡时,v正(O2)=2v逆(SO3) |
8.下列说法中错误的是( )
| A. | 历史上很多种元素是通过原子光谱发现的 | |
| B. | 鉴别晶体与非晶体,最为科学的方法是X射线衍射法 | |
| C. | 前36号元素中基态电子排布未成对电子数最多的元素,在第四周期第IIIB族 | |
| D. | 金属性越强的金属元素,第一电离能不一定就越小 |