题目内容
5.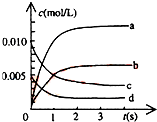 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示NO2的浓度变化曲线是b.用O2表示从0~2s内该反应的平均速率v=0.0015mol•L-1•s-1.
(3)能说明该反应已达到平衡状态的是be.
a、v (NO2)=2v (O2)
b、容器内压强保持不变
c、v逆(NO)=v正(O2)
d、容器内混合气体的密度保持不变
e、该容器内颜色保持不变.
分析 (1)由表格数据可知,3min时达到平衡,NO的物质的量为0.007mol,结合c=$\frac{n}{V}$计算;
(2)根据表格知,随着反应的进行,一氧化氮的物质的量减小,则平衡向正反应方向移动,二氧化氮的物质的量逐渐增大,根据一氧化氮和二氧化氮之间转化关系式计算平衡时二氧化氮的物质的量,从而确定曲线;先计算一氧化氮的反应速率,再根据同一化学反应中同一时间段内,各物质的反应速率之比等于其计量数之比计算氧气的反应速率;
(3)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再改变,由此衍生的一些物理量也不变.
解答 解:(1)由表格数据可知,3min时达到平衡,NO的物质的量为0.007mol,c(NO)=$\frac{0.007mol}{2L}$=0.0035mol/L,
故答案为:0.0035mol/L;
(2)根据表格知,随着反应的进行,一氧化氮的物质的量减小,则平衡向正反应方向移动,二氧化氮的物质的量逐渐增大,当反应达到平衡状态时,参加反应的n(NO)=(0.020-0.007)mol=0.013mol,根据二氧化氮和一氧化氮的关系式知,平衡状态时生成n(NO2)等于参加反应的n(NO),所以为0.013mol,c(NO2)=$\frac{0.013mol}{2L}$=0.0065mol/L;
0~2s时,v(NO)=$\frac{\frac{(0.020-0.008)mol}{2L}}{2s}$=0.003mol/(L.s),同一化学反应中同一时间段内,各物质的反应速率之比等于其计量数之比,所以v(O2)=$\frac{1}{2}$v(NO)=0.0015mol•L-1•s-1,
故答案为:b;0.0015mol•L-1•s-1;
(3)a.当v (NO2)=2v (O2)时,该反应不一定达到平衡状态,故a错误;
b.该反应是一个反应气体气体体积改变的可逆反应,当达到平衡状态时,各物质的浓度不变,则容器内压强保持不变,故b正确;
c.v逆(NO):v正(O2)=2:1时,该反应达到平衡状态,所以当v逆(NO)=v正(O2),该反应未达到平衡状态,故c错误;
d.根据质量守恒定律知,混合物质量始终不变,容器的体积不变,则容器内混合气体的密度始终不变,所以不能据此判断是否达到平衡状态,故d错误;
e.只有二氧化氮是有色气体,当反应达到平衡状态时,二氧化氮的物质的量不变,则该容器内颜色保持不变,故e正确;
故答案为:be.
点评 本题考查化学平衡的计算,题目难度中等,涉及化学平衡状态的判断、化学反应速率的计算等知识,根据v=$\frac{△c}{△t}$、v(正)=v(逆)来分析解答即可,试题培养了学生的分析能力及化学计算能力.

| A. | lmol NH2-中含有9 NA个电子 | |
| B. | 等质量的甲烷、乙烯、1,3-丁二烯分别在空气中充分燃烧,所耗用氧气的量依次减小 | |
| C. | 46g C2H5OH燃烧放出的热量为乙醇的燃烧热 | |
| D. | 常温下,56g铁粉与足量浓硝酸反应,电子转移数目为3NA |
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
①A元素在周期表中的位置第三周期第ⅥA族;②C单质分子的电子式
 ;
;③D的原子结构示意图
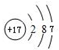 ;④电子式表示A和B元素组成的化合物的形成过程:
;④电子式表示A和B元素组成的化合物的形成过程: .
.(2)元素D与元素A相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是bde(填选项序号).
a.常温下D的单质和A的单质状态不同
b.D的氢化物比A的氢化物稳定
c.一定条件下D和A的单质都能与钠反应
d.A最高价含氧酸的酸性弱于D最高价含氧酸
e.D单质能与A的氢化物反应生成A单质
(3)X是由A、B、C、D四种元素中的某种元素组成的单质,能经图所示的过程转化为(其他条件略去).
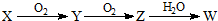
①若Y是有刺激性气味的无色气体,把Y通入BaCl2溶液中,无现象,然后滴加适量H2O2溶液,有白色沉淀生成,则该白色沉淀为BaSO4,试写出Y与H2O2溶液反应的化学方程式:SO2+H2O2=H2SO4;
②若Z是红棕色气体,则Z→W的反应中氧化剂与还原剂物质的量之比为1:2.
| A. | 可逆反应 | B. | 任何反应 | C. | 溶液间反应 | D. | 气体间反应 |
| A. | 原电池中电子流出的一极是正极 | |
| B. | 原电池是将化学能转变为电能的装置 | |
| C. | 构成原电池的正极和负极必须是两种不同的金属 | |
| D. | 原电池放电时,电流的方向是从负极到正极 |
①向2mL 0.1mol•L-1 K2Cr2O7溶液中滴入3滴6mol•L-1 NaOH溶液,溶液由橙色变为黄色;向所得溶液中再滴入5滴浓H2SO4,溶液由黄色变为橙色
②向2mL 0.1mol•L-1 酸化的K2Cr2O7溶液中滴入适量(NH4)2Fe(SO4)2溶液,溶液由橙色变为绿色,发生反应:Cr2O7 2-+14H++6Fe2+=2Cr3+(绿色)+6Fe3++7H2O.
下列分析正确的是( )
| A. | 实验①和②均能证明K2Cr2O7溶液中存在上述平衡 | |
| B. | 实验②能说明氧化性:Cr2O7 2->Fe3+ | |
| C. | CrO42- 和Fe2+在酸性溶液中可以大量共存 | |
| D. | 稀释K2Cr2O7溶液时,溶液中各离子浓度均减小 |
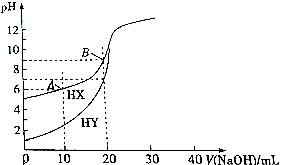
| A. | 相同条件下,HX和HY中和碱的能力相同 | |
| B. | 常温下,HX的电离平衡常数K=1×10-9mol•L-1 | |
| C. | 点存在:c(X-)-c(HX)>c(H+)-c(0H-) | |
| D. | 向B点溶液通人HCl气体至中性:c(HX)+c(Cl-)+2c(X-)=0.2mol•L-1A |
| A. | 双氧水使酸性KMnO4溶液的红色褪去:3H2O2+2MnO4-+6H+=2Mn2++4O2↑+6H2O | |
| B. | HClO4的电离方程式:HClO4=H++ClO4- | |
| C. | 碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | |
| D. | Fe2+被空气氧化:4Fe2++O2+2H2O=4Fe3++4OH- |
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ⑨ | ④ | ⑤ | ⑩ | ⑥ | ⑦ | ⑧ |
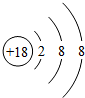 ;
;(2)表中金属性最强的元素是Na(用元素符号表示,下同),非金属性最强的元素是F,可作半导体材料的是Si元素的单质;
(3)表中能形成两性氢氧化物的元素是Al,写出该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
(4)⑨的最高价氧化物的水化物所含化学键类型离子键、共价键;
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式);
(6)元素①的最高价氧化物的电子式
 ,④元素与⑦元素形成化合物的电子式
,④元素与⑦元素形成化合物的电子式 .
.