题目内容
下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在这些元素中,最易失电子的元素是 ,非金属性最强的元素是 ;
(2)化学性质最不活泼的元素是 ,其原子的原子结构示意图为
(3)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;(填写化学式)
(4)在③~⑦元素中,原子半径最大的是 ,原子半径最小的是 ;
(5)比较①和⑥的气态氢化物的稳定性: > (填写化学式)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)化学性质最不活泼的元素是
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,原子半径最大的是
(5)比较①和⑥的气态氢化物的稳定性:
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表位置知,①~⑩号元素分别是N、F、Na、Mg、Al、Si、Cl、Ar、K、Ca元素,
(1)在这些元素中,金属性最强的元素位于元素周期表左下角,金属性越强的元素失电子越容易;非金属性最强的元素位于元素周期表右上角(稀有气体元素除外);
(2)稀有气体元素化学性质最不活泼,这几种元素中属于稀有气体元素的是Ar,Ar原子核外有3个电子层、18个电子,据此书写原子结构示意图;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强,元素金属性越强,其最高价氧化物的水化物碱性越强,呈两性的氢氧化物是Al(OH)3;
(4)在③~⑦元素中,这几种元素都是同一周期元素,原子半径随着原子序数增大而减小;
(5)元素的非金属性越强,其氢化物越稳定.
(1)在这些元素中,金属性最强的元素位于元素周期表左下角,金属性越强的元素失电子越容易;非金属性最强的元素位于元素周期表右上角(稀有气体元素除外);
(2)稀有气体元素化学性质最不活泼,这几种元素中属于稀有气体元素的是Ar,Ar原子核外有3个电子层、18个电子,据此书写原子结构示意图;
(3)元素的非金属性越强,其最高价氧化物的水化物酸性越强,元素金属性越强,其最高价氧化物的水化物碱性越强,呈两性的氢氧化物是Al(OH)3;
(4)在③~⑦元素中,这几种元素都是同一周期元素,原子半径随着原子序数增大而减小;
(5)元素的非金属性越强,其氢化物越稳定.
解答:
解:根据元素在周期表位置知,①~⑩号元素分别是N、F、Na、Mg、Al、Si、Cl、Ar、K、Ca元素,
(1)在这些元素中,金属性最强的元素位于元素周期表左下角,金属性越强的元素失电子越容易,所以最容易失电子的元素是K;非金属性最强的元素位于元素周期表右上角(稀有气体元素除外),所以非金属性最强的元素是F,故答案为:K;F;
(2)这几种元素中属于稀有气体元素的是Ar,Ar原子核外有3个电子层、18个电子,其原子结构示意图为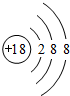 ,故答案为:Ar;
,故答案为:Ar; ;
;
(3)这几种元素中非金属性最强的是F元素,但F没有正化合价,其次是Cl元素,所以酸性最强的最高价含氧酸是HClO4,金属性最强的是K元素,所以KOH碱性最强,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;KOH;Al(OH)3;
(4)同一周期元素,原子半径随着原子序数增大而减小,所以在③~⑦元素中,原子半径最大的是Na、Z最小的是Cl元素,故答案为:Na;Cl;
(5)元素的非金属性强弱顺序是N>Si,所以氢化物越稳定NH3>SiH4,故答案为:NH3;SiH4.
(1)在这些元素中,金属性最强的元素位于元素周期表左下角,金属性越强的元素失电子越容易,所以最容易失电子的元素是K;非金属性最强的元素位于元素周期表右上角(稀有气体元素除外),所以非金属性最强的元素是F,故答案为:K;F;
(2)这几种元素中属于稀有气体元素的是Ar,Ar原子核外有3个电子层、18个电子,其原子结构示意图为
 ,故答案为:Ar;
,故答案为:Ar; ;
;(3)这几种元素中非金属性最强的是F元素,但F没有正化合价,其次是Cl元素,所以酸性最强的最高价含氧酸是HClO4,金属性最强的是K元素,所以KOH碱性最强,呈两性的氢氧化物是Al(OH)3,
故答案为:HClO4;KOH;Al(OH)3;
(4)同一周期元素,原子半径随着原子序数增大而减小,所以在③~⑦元素中,原子半径最大的是Na、Z最小的是Cl元素,故答案为:Na;Cl;
(5)元素的非金属性强弱顺序是N>Si,所以氢化物越稳定NH3>SiH4,故答案为:NH3;SiH4.
点评:本题考查了元素周期表和元素周期律综合应用,根据元素在周期表中位置确定元素性质,再结合原子结构、元素周期律来分析解答,知道元素非金属性强弱与其最高价含氧酸酸性强弱、氢化物稳定性的关系,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、草酸氢钾溶液呈酸性,在0.1mol?L-1 KHC2O4溶液中:c(C2O42-)>c(H2C2O4) |
| B、在小苏打水溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C、相同温度下,1mol?L-1氨水溶液与0.5mol?L-1氨水溶液中,c(OH-)之比是2:1 |
| D、当氨水与盐酸恰好完全反应时,c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
下列说法或表示方法正确的是( )
| A、乙烯的结构简式CH2CH2 |
| B、化学名词:乙酸乙酯、苯、油脂、坩锅 |
C、 是一种烃 是一种烃 |
D、聚乙烯的化学式为 |

