题目内容
13.(1)中国的瓷器驰名世界,制备陶瓷史以粘土[主要成分Al2Si2O5(OH)4]为原料,经高温烧结而成.若以氧化物形式表示粘土的组成,应写为Al2O3•2SiO2•2H2O.(2)天然水中杂质较多,常需加入明矾、ClO2等物质处理后才能引用,加入明矾后,其净水原理的离子方程式是A13++3H2O?Al(OH)3(胶体)+3H+.
分析 (1)根据化学式改写成相应的氧化物得形式,按照活泼金属氧化物•较活泼金属氧化物•SiO2•H2O得顺序来书写,并要遵守原子守恒来分析解答;
(2)明矾中铝离子水解生成胶体具有吸附性,则可对水质净化.
解答 解:(1)铝的氧化物为Al2O3,硅的氧化物为SiO2,氢的氧化物为H2O,
则根据活泼金属氧化物.较活泼金属氧化物.SiO2.H2O得顺序可知,
[Al2Si2O5(OH)4]可改成Al2O3•2SiO2•2H2O,
故答案为:Al2O3•2SiO2•2H2O;
(2)明矾中铝离子水解生成胶体具有吸附性,则可对水质净化,水解离子反应为A13++3H2O?Al(OH)3(胶体)+3H+,
故答案为:A13++3H2O?Al(OH)3(胶体)+3H+.
点评 本题考查将复杂化合物写出氧化物的形式、方程式是书写,明确物质的性质是解本题关键,根据反应物、生成物及反应条件书写方程式,题目难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
4.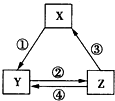 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )| 选项 | X | Y | Z |
| A | Mg | MgO | MgCl2 |
| B | Fe | FeCl3 | FeCl2 |
| C | Na2CO3 | NaOH | NaHCO3 |
| D | Cl2 | Ca(ClO)2 | HClO |
| A. | A | B. | B | C. | C | D. | D |
1.江苏省将大力实施“清水蓝天”工程.下列不利于“清水蓝天”工程实施的是( )
| A. | 大力实施矿物燃料“脱硫、脱销技术”,减少硫的氧化物和氮的氧化物污染 | |
| B. | 禁止未经处理的工业废水和生活污水的任意排放 | |
| C. | 积极推广太阳能、风能、地热能及水能等的使用,减少化石燃料的使用 | |
| D. | 大量使用化肥农药,提高粮食产量 |
8.除去下列物质中的杂质(括号内是杂质),能采用加入过量NaOH溶液充分反应再过滤的方法的是( )
| A. | FeCl2(FeCl3) | B. | KCl(NaCl) | C. | Fe2O3(Al2O3) | D. | NaCl(MgCl2) |
18.某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定.第一组,取刚降到地面的酸雨水样,进行了如下实验:
①将一片红色的玫瑰花瓣浸在一份水样中;
②向雨水试样中滴加氯化钡溶液,有白色沉淀生成;
③每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
(1)一段时间后,观察到玫瑰花瓣红色变浅,原因是SO2有漂白作用.
(2)生成白色沉淀的离子方程式Ba2++SO42-=BaSO4↓.
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)2SO2+2H2O+O2=2H2SO4.
第二组,拟用如图装置定量分析空气中SO2的含量:

(4)通入空气前应进行的实验操作是气密性检查;KMnO4溶液中导管末端做成球状多孔结构的作用是增大接触面积,有利于SO2的充分吸收.
(5)已知:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+.随着空气的不断通入,酸性高锰酸钾的溶液逐渐变浅直至褪色,说明SO2具有还原性性.
(6)若实验中气体流速aL•min-1,酸性KMnO4溶液的体积bL,其浓度为cmol•L-1,从气体通入到紫色恰好褪去,用时5min.则空气中二氧化硫的含量为$\frac{32bc}{a}$g•L-1.
①将一片红色的玫瑰花瓣浸在一份水样中;
②向雨水试样中滴加氯化钡溶液,有白色沉淀生成;
③每隔一定时间测定其pH,数据如表Ⅰ所示.
表Ⅰ不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(2)生成白色沉淀的离子方程式Ba2++SO42-=BaSO4↓.
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示)2SO2+2H2O+O2=2H2SO4.
第二组,拟用如图装置定量分析空气中SO2的含量:

(4)通入空气前应进行的实验操作是气密性检查;KMnO4溶液中导管末端做成球状多孔结构的作用是增大接触面积,有利于SO2的充分吸收.
(5)已知:5SO2+2MnO4-+2H2O═5SO42-+2Mn2++4H+.随着空气的不断通入,酸性高锰酸钾的溶液逐渐变浅直至褪色,说明SO2具有还原性性.
(6)若实验中气体流速aL•min-1,酸性KMnO4溶液的体积bL,其浓度为cmol•L-1,从气体通入到紫色恰好褪去,用时5min.则空气中二氧化硫的含量为$\frac{32bc}{a}$g•L-1.
5.用放射性同位素${\;}_{16}^{35}$S对杀虫剂进行标记,可跟踪杀虫剂的污染途径.该原子的中子数是( )
| A. | 16 | B. | 35 | C. | 19 | D. | 51 |
2.下列离子方程式的书写正确的是( )
| A. | 大理石与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铜和硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| C. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 硫酸与氢氧化钡溶液反应:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
3.1.5g 火箭燃料二甲基肼(CH3-NH-NH-CH3)完全燃烧放出50kJ热量,则二甲基肼的燃烧热为( )
| A. | 2000kJ | B. | △H=-2000kJ/mol | C. | △H=-1500kJ/mol | D. | -2000kJ/mol |
