题目内容
(1)0.5mol H2SO4 的质量是 g,能和 mol NaOH完全反应,该硫酸所含氢元素的质量与 mol H3PO4或标准状况下 L HCl中所含氢元素的质量相同;
(2)将11.2g纯净的铁粉投入到200mL 足量的稀盐酸中,完全反应后能够放出标准状况下的气体体积为 ,实验后所得溶液中Fe2+的物质的量浓度为 .
(2)将11.2g纯净的铁粉投入到200mL 足量的稀盐酸中,完全反应后能够放出标准状况下的气体体积为
考点:物质的量的相关计算,气体摩尔体积,物质的量浓度的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)结合m=nM、V=nVm、N=nNA及分子构成、酸碱中和计算;
(2)n(Fe)=
=0.2mol,由Fe+2HCl=FeCl2+H2↑可知,n(Fe)=n(Fe2+)=n(H2),结合V=nVm、c=
计算.
(2)n(Fe)=
| 11.2g |
| 56g/mol |
| n |
| V |
解答:
解:(1)0.5mol H2SO4 的质量是0.5mol×98g/mol=49g,含1molH+,能和1mol NaOH完全反应,该硫酸所含氢元素的质量与
mol H3PO4或标准状况下22.4L HCl中所含氢元素的质量相同,均为1g,
故答案为:49;1;
;22.4;
(2)n(Fe)=
=0.2mol,由Fe+2HCl=FeCl2+H2↑可知,n(Fe)=n(Fe2+)=n(H2),标准状况下的气体体积为0.2mol×22.4L/mol=4.48L,所得溶液中Fe2+的物质的量浓度为c=
=
=1mol/L,
故答案为:4.48;1mol/L.
| 1 |
| 3 |
故答案为:49;1;
| 1 |
| 3 |
(2)n(Fe)=
| 11.2g |
| 56g/mol |
| n |
| V |
| 0.2mol |
| 0.2L |
故答案为:4.48;1mol/L.
点评:本题考查物质的量的计算,为高频考点,把握以物质的量为中心的计算公式为解答的关键,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
相关题目
在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol N气体混合,发生如下反应:2M(g)+3N(g)?x Q(g)+3R(g),该反应达平衡时,生成2.4mol R,并测得Q的浓度为0.4mol/L,下列有关叙述正确的是( )
| A、x值为2 |
| B、混合气体的密度增大 |
| C、平衡时N的浓度为0.3 mol/L |
| D、N的转化率为60% |
设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是( )
| A、1mol任何粒子所含的原子总数均约为NA |
| B、常温常压下,11.2 L氧气所含的原子数为NA |
| C、常温常压下,48g O3所含的氧原子数为3NA |
| D、标准状况下,22.4 L H2O含有的分子数为NA |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、过量的铁与1mol干燥的氯气充分反应,转移的总电子数为2NA |
| B、1L 1mol/L的氯化铁溶液完全反应生成氢氧化铁胶体,则氢氧化铁胶粒数小于NA |
| C、100g 17%的氨水溶液中含有的氨气分子数为NA |
| D、125g CuSO4?5H2O晶体中含有0.5 NA个Cu2+ |
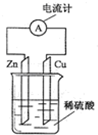 如图所示的原电池装置
如图所示的原电池装置