题目内容
某CuO粉末中混有少量Cu2O.有一个课外活动小组利用如图所示装置测定其中Cu2O的含量.根据图示内容回答下列问题:
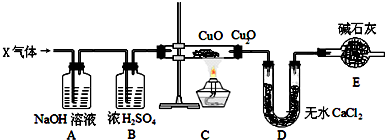
(1)气体X是常见还原剂CO、H2中的一种,请根据组合装置判断X是 .
(2)装置B的作用是 ,若缺少B装置,将直接导致测定出的质量偏 (填大、小).
(3)已知反应前CuO和Cu2O的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g,则原混合物中Cu2O的质量为 g.
(4)装置E的作用是 .
(5)反应后,装置C中只有Cu,写出Cu2O与气体X反应的化学方程式, .其中氧化剂是 ,被氧化的元素是 .

(1)气体X是常见还原剂CO、H2中的一种,请根据组合装置判断X是
(2)装置B的作用是
(3)已知反应前CuO和Cu2O的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g,则原混合物中Cu2O的质量为
(4)装置E的作用是
(5)反应后,装置C中只有Cu,写出Cu2O与气体X反应的化学方程式,
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)该题是一道综合实验题,由题意可知,实验目的是测定氧化铜和氧化亚铜混合物中氧化亚铜的含量,反应原理是利用还原性气体夺氧.氢气夺氧生成的水被氯化钙吸收,D装置质量增加量为生成的水的质量.已知氧化铜和氧化亚铜混合物的质量和生成水的质量,根据相关的化学方程式就可求出氧化亚铜的质量,确定混合物中其含量;
(2)由题意知氢气中混有水蒸气和二氧化碳气体,若不除去,测得水的质量就会有偏差,为此在氢气夺氧前必须将其除去,干燥用装置B中浓硫酸,除二氧化碳用装置A中氢氧化钠溶液,在除二氧化碳时因从溶液里经过,必定带出水蒸气,所以要把干燥放在其后进行;
(3)已知反应前混合物的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g为水的质量,设原混合物中 Cu2O的质量为X,它与H2反应生成水的质量为Y,那么CuO的质量为:m1g-X,它与H2反应生成水的质量为m2g-Y,依据化学方程式定量关系计算得到;
(4)当D与外界连通时,氯化钙会吸收空气中的水蒸气,使测得水的质量出现偏差,所以加E装置,用以防止空气中的水蒸气进入D装置,使实验数据更准确;
(5)Cu2O在加热的条件下也能被X气体还原为Cu,氧化亚铜做还原剂被还原.
(2)由题意知氢气中混有水蒸气和二氧化碳气体,若不除去,测得水的质量就会有偏差,为此在氢气夺氧前必须将其除去,干燥用装置B中浓硫酸,除二氧化碳用装置A中氢氧化钠溶液,在除二氧化碳时因从溶液里经过,必定带出水蒸气,所以要把干燥放在其后进行;
(3)已知反应前混合物的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g为水的质量,设原混合物中 Cu2O的质量为X,它与H2反应生成水的质量为Y,那么CuO的质量为:m1g-X,它与H2反应生成水的质量为m2g-Y,依据化学方程式定量关系计算得到;
(4)当D与外界连通时,氯化钙会吸收空气中的水蒸气,使测得水的质量出现偏差,所以加E装置,用以防止空气中的水蒸气进入D装置,使实验数据更准确;
(5)Cu2O在加热的条件下也能被X气体还原为Cu,氧化亚铜做还原剂被还原.
解答:
解:(1)A装置中盛放浓烧碱溶液,能与二氧化碳反应,其作用是除去H2中的CO2气体,D装置的作用是吸收X气体夺氧后生成的气体,由D装置盛放氯化钙干燥剂可知,吸收的是水,所以X气体为氢气,化学式为H2,故答案为:H2;
(2)B装置中盛放浓硫酸,浓硫酸具有吸水性,其作用是干燥H2 ,若缺少它,氢气携带的水蒸气经过C装置也会进入D装置,被氯化钙吸收,使测得水的质量出现偏差.所以若缺少它,将直接导致反应后D装置内的物质的质量偏小,
故答案为:干燥气体;小;
(3)已知反应前混合物的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g为水的质量,设原混合物中 Cu2O的质量为X,它与H2反应生成水的质量为Y,那么CuO的质量为:m1g-X,它与H2反应生成水的质量为m2g-Y.
CuO+H2
Cu+H2O
80 18
m1g-X m2g-Y
Cu2O+H2
2Cu+H2O
144 18
X Y
18(m1g-X)=80(m2g-Y)
144Y=18X
解方程组得:X=
m1-10m2 ;
所以原混合物中Cu2O的质量为
m1-10m2 g,
故答案为:
m1-10m2 ;
(4)当D与外界连通时,氯化钙会吸收空气中的水蒸气,使测得水的质量出现偏差,所以加E装置,用以防止空气中的水蒸气进入D装置,使实验数据更准确;
故答案为:防止空气中的水蒸气进入D;
(5)Cu2O在加热的条件下也能被X气体还原为Cu,Cu2O+H2
2Cu+H2O,氧化亚铜做还原剂被还原,氢元素被氧化;
故答案为:Cu2O+H2
2Cu+H2O;Cu2O;H.
(2)B装置中盛放浓硫酸,浓硫酸具有吸水性,其作用是干燥H2 ,若缺少它,氢气携带的水蒸气经过C装置也会进入D装置,被氯化钙吸收,使测得水的质量出现偏差.所以若缺少它,将直接导致反应后D装置内的物质的质量偏小,
故答案为:干燥气体;小;
(3)已知反应前混合物的总质量为m1 g,完全反应后U型管内物质的质量增加了m2 g为水的质量,设原混合物中 Cu2O的质量为X,它与H2反应生成水的质量为Y,那么CuO的质量为:m1g-X,它与H2反应生成水的质量为m2g-Y.
CuO+H2
| ||
80 18
m1g-X m2g-Y
Cu2O+H2
| ||
144 18
X Y
18(m1g-X)=80(m2g-Y)
144Y=18X
解方程组得:X=
| 9 |
| 4 |
所以原混合物中Cu2O的质量为
| 9 |
| 4 |
故答案为:
| 9 |
| 4 |
(4)当D与外界连通时,氯化钙会吸收空气中的水蒸气,使测得水的质量出现偏差,所以加E装置,用以防止空气中的水蒸气进入D装置,使实验数据更准确;
故答案为:防止空气中的水蒸气进入D;
(5)Cu2O在加热的条件下也能被X气体还原为Cu,Cu2O+H2
| ||
故答案为:Cu2O+H2
| ||
点评:该题是一道综合实验题,实验设计严密,考查的知识点较多,解题的关键是明确实验目的和原理,分析综合装置各部分的作用

练习册系列答案
相关题目
设阿伏加德罗常数为NA,则下列说法正确的是( )
| A、15g甲基(-CH3)所含有的电子数是10NA | ||
| B、0.5mol 1,3一丁二烯分子中含有的碳碳双键数为NA | ||
C、标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| D、60gSiO2晶体中,含有NA个Si-O键 |
下列物质的检验或提纯,其结论或方法正确的是( )
| A、某物质中加入BaCl2溶液产生白色沉淀加入稀HNO3后白色沉淀不溶解,说明该溶液中含有Ag+或SO42-中的至少一种 |
| B、CO2混有少量HC1.可用饱和NaHCO3除去 |
| C、Cl2中混有少量HCl可用通入饱和NaCl溶液的方法除去 |
| D、N2混有少量NO2,可用水洗法除去 |
 如图所示,甲、乙为互相串联的两个电解池.请回答
如图所示,甲、乙为互相串联的两个电解池.请回答 如图所示X、Y分别为直流电源的两极,Z溶液可能为:①稀硫酸 ②NaOH溶液 ③Na2SO4 溶液 ④CuCl2 溶液 ⑤NaCl溶液 ⑥稀盐酸 ⑦CuSO4 溶液
如图所示X、Y分别为直流电源的两极,Z溶液可能为:①稀硫酸 ②NaOH溶液 ③Na2SO4 溶液 ④CuCl2 溶液 ⑤NaCl溶液 ⑥稀盐酸 ⑦CuSO4 溶液


 分子中的亲水基是:
分子中的亲水基是: LED晶片在文化传媒中有着广泛的应用.目前市售LED晶片,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.
LED晶片在文化传媒中有着广泛的应用.目前市售LED晶片,材质基本以AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主.