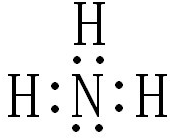题目内容
19.分类法在化学学科的研究中起到了非常重要的作用.下列分类标准不合理的是( )①根据组成元素将氧化物分成酸性氧化物和碱性氧化物
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据是否有丁达尔现象将分散系分为溶液和胶体
④根据水溶液是否能完全电离将电解质分为强电解质和弱电解质.
| A. | ②③ | B. | ②④ | C. | ①③ | D. | ① |
分析 ①根据氧化物的性质分类,是氧化物与酸、碱的反应情况进行分类,将氧化物分成酸性氧化物、碱性氧化物、两性氧化物、不成盐氧化物;
②根据反应中是否有电子转移将化学反应分为是氧化还原反应和非氧化还原反应;
③根据分散系的分类依据是分散质微粒直径大小;
④电解质在水溶液中完全电离,而弱电解质电离不完全.
解答 解:①根据氧化物的性质将氧化物分成和碱反应生成盐和水的氧化物为酸性氧化物,和酸反应生成盐和水的氧化物为碱性氧化物,和酸、碱都反应生成盐和水的氧化物为两性氧化物,和酸、碱都不反应的氧化物为不成盐氧化物,故①错误;
②根据反应中是否有盐酸化合价变化,是否有电子转移将化学反应分为是氧化还原反应和非氧化还原反应,故②正确;
③丁达尔现象是胶体的性质,根据分散系分散质微粒大小将分散系分为:分散质微粒直径小于1nm形成的分散系为溶液,分散质微粒直径1nm-100nm形成的分散系为胶体,分散质微粒直径大于100nm形成的分散系为浊液,故③错误;
④电解质在水溶液中完全电离,而弱电解质电离不完全,根据电解质在水溶液中能否完全电离将电解质分为强电解质和弱电解质,故④正确;
故选C.
点评 本题考查物质的分类,题目难度不大,注意物质的分类的依据,不同的分类标准会得出不同的分类结果,注意概念的实质理解.

练习册系列答案
相关题目
9.氧化铁是一种红色的颜料,在工业上常以富含硫酸亚铁的废液为原料生产氧化铁,其主要流程如下:
废液$→_{①}^{提纯、结晶}$FeSO4•7HO2$\stackrel{②}{→}$FeSO4溶液$→_{③}^{NH_{4}HCO_{3}溶液}$FeCO3$\stackrel{④}{→}$Fe2CO3
已知步骤①中硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示.
若从硫酸亚铁溶液中结晶出FeSO4•7H2O,控制的温度(t)为t<56.7℃;
(1)步骤②需加一定量硫酸,其主要目的是抑制FeSO4的水解;
(2)生产FeCO3浊液的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;
(3)FeCO3浊液露置在空气中会出现红褐色的固体,该变化的化学方程式为4FeCO3+6H2O+O2═4Fe(OH)3+4CO2;
(4)已知FeSO4•7H2O晶体在加热条件下发生反应,其中一种生成物会用于涂料中的着色剂.请写出
FeSO4•7H2O分解的反应式FeSO4•7H2O$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑+14H2O↑;利用如图装置可检验该反应的气体产物.
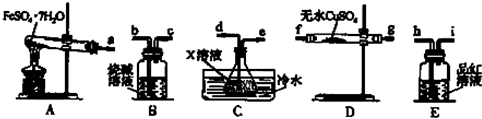
请填写下列空白:
①仪器的连接顺序为a 接f(或g)、g(或f)接d、e接h、i接b;
②装置C中的X为氯化钡溶液.
废液$→_{①}^{提纯、结晶}$FeSO4•7HO2$\stackrel{②}{→}$FeSO4溶液$→_{③}^{NH_{4}HCO_{3}溶液}$FeCO3$\stackrel{④}{→}$Fe2CO3
已知步骤①中硫酸亚铁在不同温度下的溶解度和析出晶体的组成如下表所示.
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 | ||
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27.0 | ||
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||||
(1)步骤②需加一定量硫酸,其主要目的是抑制FeSO4的水解;
(2)生产FeCO3浊液的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;
(3)FeCO3浊液露置在空气中会出现红褐色的固体,该变化的化学方程式为4FeCO3+6H2O+O2═4Fe(OH)3+4CO2;
(4)已知FeSO4•7H2O晶体在加热条件下发生反应,其中一种生成物会用于涂料中的着色剂.请写出
FeSO4•7H2O分解的反应式FeSO4•7H2O$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑+14H2O↑;利用如图装置可检验该反应的气体产物.

请填写下列空白:
①仪器的连接顺序为a 接f(或g)、g(或f)接d、e接h、i接b;
②装置C中的X为氯化钡溶液.
7.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:K+、Cl-、NO3-、Fe3+ | |
| B. | 能使甲基橙显红色的溶液:CO32-、Na+、Cl-、SO42- | |
| C. | pH=1的溶液中:Mg2+、SO42-、Fe2+、Cu2+ | |
| D. | 能使铝钝化的溶液中:Ba2+、Na+、Cl-、I- |
14.FeS与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为1:1:1时,实际参加反应的FeS与HNO3的物质的量之比为( )
| A. | 1:6 | B. | 2:15 | C. | 2:11 | D. | 1:7 |
4.高中化学学习过程中的物质颜色是需要注意的.下列关于颜色的描述正确的个数是( )
①氯水放久了会逐渐由黄绿色变成几乎无色
②用硝酸银检验Br-会产生AgBr难溶于水的白色沉淀
③KI溶液中加入淀粉溶液会变成蓝色
④溴水中加入CCl4振荡静置后,上层为橙红色
⑤实验室的浓硝酸溶液久置呈黄色.
①氯水放久了会逐渐由黄绿色变成几乎无色
②用硝酸银检验Br-会产生AgBr难溶于水的白色沉淀
③KI溶液中加入淀粉溶液会变成蓝色
④溴水中加入CCl4振荡静置后,上层为橙红色
⑤实验室的浓硝酸溶液久置呈黄色.
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
11.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 22.4 L N2和NH3混合气体中原子间共有3NA个共用电子对 | |
| B. | 3.0 g甲醛HCHO和乙酸混合物中共含碳原子数为0.1NA | |
| C. | 25℃时pH=1的醋酸溶液中含有H+的数目为0.1NA | |
| D. | 标准状况下,2.24 L CH2Cl2含有的分子数为0.1NA |
9.下列溶液中粒子的物质的量浓度关系正确的是( )
| A. | 0.1mol/L NH4HCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | 20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/LHCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
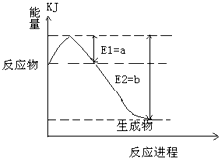 合成氨工业对国民经济和社会发展具有重要意义
合成氨工业对国民经济和社会发展具有重要意义