题目内容
①1molH2O约含 个H2O;
②1molO约含 个e-;
③3×6.02×1023个电子的物质的量是 mol e-;
④1.204×1024个水分子的物质的量为 mol.
②1molO约含
③3×6.02×1023个电子的物质的量是
④1.204×1024个水分子的物质的量为
考点:物质的量的相关计算
专题:
分析:①根据N=nNA计算;
②每个氧原子含有8个电子,氧原子含有电子物质的量为氧原子的8倍,根据N=nNA计算;
③根据n=
计算;
④根据n=
计算.
②每个氧原子含有8个电子,氧原子含有电子物质的量为氧原子的8倍,根据N=nNA计算;
③根据n=
| N |
| NA |
④根据n=
| N |
| NA |
解答:
解:①1molH2O含有分子数目为1mol×6.02×1023mol-1=6.02×1023,故答案为:6.02×1023;
②每个氧原子含有8个电子,氧原子含有电子物质的量为氧原子的8倍,含有电子数目为,1mol×8×6.02×1023mol-1=8×6.02×1023,故答案为:8×6.02×1023;
③3×6.02×1023个电子的物质的量是
=3mol,故答案为:3;
④1.204×1024个水分子的物质的量为
=2mol,故答案为:2.
②每个氧原子含有8个电子,氧原子含有电子物质的量为氧原子的8倍,含有电子数目为,1mol×8×6.02×1023mol-1=8×6.02×1023,故答案为:8×6.02×1023;
③3×6.02×1023个电子的物质的量是
| 3×6.02×1023 |
| 6.02×1023mol-1 |
④1.204×1024个水分子的物质的量为
| 1.204×1024 |
| 6.02×1023mol-1 |
点评:本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关甲酯.

练习册系列答案
相关题目
下列各装置中,不能构成原电池的是(电解质都为稀硫酸)( )
A、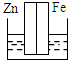 |
B、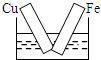 |
C、 |
D、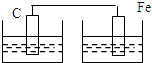 |
下列物质中,摩尔质量最大的是 ( )
| A、10mL H2O |
| B、0.1mol HCl |
| C、24g Mg |
| D、1g CaCO3 |
下列离子方程式正确的是( )
| A、氯气通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2 HCO3-=CaCO3↓+CO32-+2H2O |
| C、向CuSO4溶液中加入Ba(OH)2溶液,观察到有蓝色沉淀生成:Cu2++2OH-=Cu(OH)2↓ |
| D、FeSO4溶液中加H2O2溶液:Fe2++2H2O2+4H+=Fe3++4H2O |
下列表达式书写正确的是( )
| A、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
| B、HCO3-的水解方程式:HCO3-+H2O?H3O++CO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、BaSO4的沉淀溶解平衡表达式:BaSO4(s)?Ba2+(aq)+SO42-(aq) |
下列离子方程式正确的是( )
| A、NaAlO2溶液中通入足量的CO2:2AlO2-+CO2+3H2O?2Al(OH)3↓+CO32- |
| B、NaHCO3溶液中滴加过量Ca(OH)2溶液:Ca2++OH-+HCO3-?CaCO3↓+H2O |
| C、硫酸铝溶液中加入过量氨水:Al3++4NH3?H2O?AlO2-+4NH4++2H2O |
| D、NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO42-?BaSO4↓+H2O |