题目内容
下列物质中,所含氢原子的数目最大的是( )
| A、18g冰 |
| B、标准状况下22.4 L H2 |
| C、50g硫酸 |
| D、6.02×1023个氨分子 |
考点:物质分子中的原子个数计算
专题:计算题
分析:根据N=nNA可知,氢原子的物质的量越大,含有的氢原子的说明越多,先计算出各物质中含有的氢原子的物质的量,然后根据H原子的物质的量大小进行判断即可.
解答:
解:A.18冰中含有水的物质的量为1mol,含有2mol氢原子;
B.标准状况下,22.4L氢气的物质的量为1mol,1mol氢气含有2mol氢原子;
C.50g硫酸的物质的量为:
=
mol,含有氢原子的物质的量为:
mol×2=
mol;
D.6.02×1023个氨分子中含有1mol氨气,含有3mol氢原子;
根据以上计算可知,含有氢原子的物质的量最大的是D,所以含有氢原子数目最多的为D,
故选D.
B.标准状况下,22.4L氢气的物质的量为1mol,1mol氢气含有2mol氢原子;
C.50g硫酸的物质的量为:
| 50g |
| 98g/mol |
| 25 |
| 49 |
| 25 |
| 49 |
| 50 |
| 49 |
D.6.02×1023个氨分子中含有1mol氨气,含有3mol氢原子;
根据以上计算可知,含有氢原子的物质的量最大的是D,所以含有氢原子数目最多的为D,
故选D.
点评:本题考查了有关物质的量的简单计算,题目难度不大,明确物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的转化关系是解答本题的关键.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
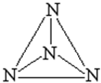 意大利科学家获得了极具研究价值的N4(分子结构如图所示),以下有关物质结构的说法正确的是( )
意大利科学家获得了极具研究价值的N4(分子结构如图所示),以下有关物质结构的说法正确的是( )| A、N均是以SP3杂化,N-N均为σ键 |
| B、N的电负性大于O,所以NH3的沸点低于H2O |
| C、N4为原子晶体,每个N的配位数为3 |
| D、N原子核外有5个未成对电子 |
下列各组物质,属于电解质的是( )
| A、NaCl |
| B、铜 |
| C、蔗糖 |
| D、CO2 |
同温同压下,含相同原子数的下列气体,密度最大的是( )
| A、SO2 |
| B、CO2 |
| C、HCl |
| D、CH4 |
香草醛是由愈创木酚为原料合成的,合成路线如图所示:下列说法正确的是( )
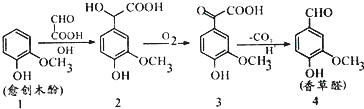

| A、等物质的量的四物质与足量NaOH溶液反应,消耗NaOH物质的量比为1:3:2:1 |
| B、化合物2在一定条件下可发生加聚反应 |
| C、检验制得的香草醛中是否混有化合物3,可用氯化铁溶液 |
| D、理论上反应1→2中原子利用率100% |
下列说法不正确的是( )
| A、手机上用的锂离子电池属于二次电池 |
| B、测定中和反应的反应热,需要记录体系达到的最终温度 |
| C、催化剂能加快化学反应速率是因为降低了反应的活化能,增大了活化分子百分率 |
| D、温度对化学平衡的影响是通过改变平衡常数实现的 |
下列叙述正确的是( )
| A、分解反应一定是氧化还原反应 |
| B、氧化还原反应的特征:化合价发生变化 |
| C、还原剂就是反应中被还原的物质 |
| D、在氧化还原反应中,失去电子的元素化合价降低 |
鼠尾草酚可用于防治骨质疏松,鼠尾草酸可两步转化得到鼠尾草酚,下列说法正确的是( )
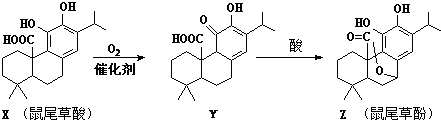

| A、X、Y、Z互为同分异构体 |
| B、1mol X与NaOH溶液反应最多消耗3mol NaOH |
| C、X、Y、Z分子中均含有2个手性碳原子 |
| D、X、Y均能与FeCl3溶液发生显色反应 |