题目内容
在Mg(NO3)2和Al(NO3)3的混合溶液中,NO3-的物质的量为0.7mol.向该溶液中加入100ml 8mol?L-1的KOH溶液,使之充分反应,反应前,若Al3+的物质的量与混合溶液中离子总物质的量的比值为x.
(不考虑Mg2+和Al3+的水解及水的电离所引起的离子总数的变化)
(1)x的取值范围是 .
(2)当KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的取值范围 .
(3)将(2)中的x值记为x1,则:
当0<x<x1时,反应生成的沉淀物的化学式为 .
当x>x1时反应生成的沉淀物的化学式为
(4)若反应前Al3+的物质的量为a mol,则a= (用含x的代数式表示).
(不考虑Mg2+和Al3+的水解及水的电离所引起的离子总数的变化)
(1)x的取值范围是
(2)当KOH刚好完全消耗,且Al3+全部转化为AlO2-时,x的取值范围
(3)将(2)中的x值记为x1,则:
当0<x<x1时,反应生成的沉淀物的化学式为
当x>x1时反应生成的沉淀物的化学式为
(4)若反应前Al3+的物质的量为a mol,则a=
考点:有关混合物反应的计算
专题:计算题
分析:(1)当溶液中完全为硝酸铝时,Al3+的物质的量与混合溶液中离子总物质的量的比值x有最大值,据此计算x的取值范围;
(2)当KOH刚完全消耗且Al3+全部转换成AlO2-时,此时溶液中溶质为KNO3、KAlO2,根据守恒可知n(K+)=n(NO3-)+n(AlO2-),n(AlO2-)=n(Al3+),利用电荷守恒计算n(Mg2+),据此计算x的值;
(3)当0<x≤0.1时,氢氧化钾过量,生成的沉淀只有Mg(OH)2;当0.1<x<0.25时,氢氧化钾不足,生成的沉淀为Al(OH)3和Mg(OH)2;
(4)设溶液中Al3+的物质的量为a mol,利用电荷守恒用a表示出Mg2+的物质的量,溶液中离子总的物质的量为三种离子之和,也等于
mol,据此列等式计算a的值(用x表示).
(2)当KOH刚完全消耗且Al3+全部转换成AlO2-时,此时溶液中溶质为KNO3、KAlO2,根据守恒可知n(K+)=n(NO3-)+n(AlO2-),n(AlO2-)=n(Al3+),利用电荷守恒计算n(Mg2+),据此计算x的值;
(3)当0<x≤0.1时,氢氧化钾过量,生成的沉淀只有Mg(OH)2;当0.1<x<0.25时,氢氧化钾不足,生成的沉淀为Al(OH)3和Mg(OH)2;
(4)设溶液中Al3+的物质的量为a mol,利用电荷守恒用a表示出Mg2+的物质的量,溶液中离子总的物质的量为三种离子之和,也等于
| a |
| x |
解答:
解:(1)当完全为Al(NO3)3时,x有最大值,硝酸根离子的物质的量为0.7mol,则铝离子的物质的量为:0.7mol×
=
mol,
则:x=
=0.25,由于是硝酸镁和硝酸铝的混合物,则x<0.25,
所以x的范围为:0<x<0.25,
故答案为:0<x<0.25;
(2)当KOH刚完全消耗且Al3+全部转换成AlO2-时,此时溶液中溶质为KNO3、KAlO2,根据守恒可知:n(K+)=n(NO3-)+n(AlO2-),故n(AlO2-)=0.1L×8mol/L-0.7mol=0.1mol,故:n(Al3+)=0.1mol,根据电荷守恒可知,n(Mg2+)=
=
=0.2mol,
则:x=
=0.1,
故答案为:0.1;
(3)当0<x≤0.1时,氢氧化钾过量,铝离子完全转化成AlO2-,生成的沉淀为Mg(OH)2;
当0.1<x<0.25时,氢氧化钾不足,生成的沉淀为Al(OH)3和Mg(OH)2的混合物,
故答案为:Mg(OH)2;Al(OH)3和Mg(OH)2;
(4)设溶液中Al3+的物质的量为a mol,由电荷守恒可知Mg2+的物质的量为:
,溶液中离子总的物质的量为三种离子之和,也等于
mol,
故:
+amol+0.7mol=
mol,
解得:a=
,
故答案为:
.
| 1 |
| 3 |
| 7 |
| 30 |
则:x=
| ||
|
所以x的范围为:0<x<0.25,
故答案为:0<x<0.25;
(2)当KOH刚完全消耗且Al3+全部转换成AlO2-时,此时溶液中溶质为KNO3、KAlO2,根据守恒可知:n(K+)=n(NO3-)+n(AlO2-),故n(AlO2-)=0.1L×8mol/L-0.7mol=0.1mol,故:n(Al3+)=0.1mol,根据电荷守恒可知,n(Mg2+)=
| 0.7mol-3n(Al3+) |
| 2 |
| 0.7mol-3×0.1mol |
| 2 |
则:x=
| 0.1mol |
| 0.1mol+0.2mol+0.7mol |
故答案为:0.1;
(3)当0<x≤0.1时,氢氧化钾过量,铝离子完全转化成AlO2-,生成的沉淀为Mg(OH)2;
当0.1<x<0.25时,氢氧化钾不足,生成的沉淀为Al(OH)3和Mg(OH)2的混合物,
故答案为:Mg(OH)2;Al(OH)3和Mg(OH)2;
(4)设溶液中Al3+的物质的量为a mol,由电荷守恒可知Mg2+的物质的量为:
| 0.7mol-3a |
| 2 |
| a |
| x |
故:
| 0.7mol-3a |
| 2 |
| a |
| x |
解得:a=
| 2.1x |
| x+2 |
故答案为:
| 2.1x |
| x+2 |
点评:本题考查混合物的有关计算,题目难度较大,注意利用守恒进行的计算,(3)为难点、易错点,需要根据(1)(2)的计算结果及铝离子的物质的量范围讨论生成沉淀情况,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质中,按其成分能与玻璃、水泥、陶瓷归于一类的是( )
| A、硅石 | B、碳化硅 |
| C、硅酸钠 | D、二氧化硅 |
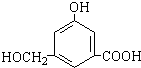 如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式:
如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式: 50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题.
50mL1.0mol/L盐酸跟50mL1.1mol/L氢氧化钠溶液在如图装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题.