题目内容
6.下列有关比较,顺序排列错误的是( )| A. | 原子半径:Al>Mg>Na | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 熔点:纯铁>铝>铝合金 |
分析 A.同一周期中,原子序数越大,原子半径越小;
B.非金属性越强,最高价氧化物对应水合物的酸性越强,结合同一周期中原子序数越大、非金属性越强分析;
C.金属性越强,最高价氧化物对应水合物的碱性越强,结合同一周期中原子序数越大、金属性越弱分析;
D.金属晶体中,电荷越高,离子半径越小,熔点高,且合金比其各成分的熔点都低.
解答 解:A.Na、Mg、Al位于同一周期,原子序数越大,原子半径越小,则原子半径:Al<Mg<Na,故A错误;
B.同一周期中原子序数越大,非金属性越强,则非金属性:Cl>S>P,非金属性越强,最高价含氧酸的酸性越强,则酸性:HClO4>H2SO4>H3PO4,故B正确;
C.Na、Mg、Al位于同一周期,原子序数越大,金属性越弱,则金属性Al<Mg<Na,金属性越强,最高价氧化物对应水合物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.合金的熔点较低,铁的熔点大于铝,则熔点:纯铁>铝>铝合金,故D周期;
故选A.
点评 本题考查了元素周期律的综合应用,题目难度不大,明确原子结构与元素周期律的关系为解答关键,注意熟练掌握元素周期律内容及应用,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.有甲、乙两个装置,下列说法错误的是( )


| A. | 甲、乙装置中,Zn的质量均减小 | B. | 甲、乙装置中,Cu上均有气泡产生 | ||
| C. | 化学反应速率 乙>甲 | D. | 甲中H+移向Zn,乙中SO42-移向Zn |
17.分类是化学研究中常用的方法.下列分类方法中,不正确的是( )
| A. | 依据分散质微粒的大小,可将化合物分为酸、碱、盐等 | |
| B. | 依据电子转移与否,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 依据化合物本身在熔融状态或化合物的水溶液是否导电,可将其分为电解质和非电解质 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
14.除去氯化铁中混有的氯化铝,最适宜的试剂组是( )
| A. | NaOH溶液、盐酸 | B. | NaOH溶液、硫酸 | C. | 氨水、NaOH溶液 | D. | 氨水、盐酸 |
1.下列关于铁和铝的性质叙述错误的是( )
| A. | 补血剂中含有+2价铁元素 | |
| B. | 铁粉和氧化铝的混合物叫铝热剂,反应时放出大量热 | |
| C. | 铝是人体中的一种微量元素,如果摄入量过多,易患老年痴呆症 | |
| D. | 铝的金属活动性比铁的金属活动性强 |
11.在实验室配制氯化亚铁溶液时,如果出现浑浊,采取的最好措施是( )
| A. | 加入锌粒 | B. | 加入铁钉 | C. | 加入盐酸 | D. | 加入硫氰化钾 |
18.下列仪器中不属于计量仪器的是( )
| A. | 量筒 | B. | 滴定管 | C. | 温度计 | D. | 烧杯 |
15.锌-碳硫酸原电池(如图)工作时,下列叙述正确的是( )
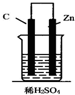

| A. | 正极反应为:Zn-2e-═Zn2+ | |
| B. | 电池反应式为:Zn+2H+═Zn2++H2↑ | |
| C. | 在闭合电路中,电子从碳极流向锌极 | |
| D. | 溶液中的H+移向锌极 |