题目内容
(8分)在密闭容器中,将1.0molCO与1.0molH2O混合加热到800℃,发生下列反应:CO(g)+H2O(g) CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
(1)达到平衡时CO2的物质的量分数为 ,该反应的化学平衡常数为 ;
(2)向该平衡体系中通入1.0mol水蒸气,达到新的平衡状态时,水蒸气的物质的量为
CO的转化率为 。
(1)25% 1;(2)1.33mol 66.7%。
【解析】
试题分析:由于开始时CO的物质的量是1.0mol,反应达到平衡,测得CO的物质的量为0.5mol,所以反应消耗的CO的物质的量是0.5mol,根据方程式中物质的量的关系可知达到平衡时产生的CO2的物质的量是0.5mol,H2的物质的量是0.5mol,H2O的平衡物质的量也是0.5mol,则达到平衡时CO2的物质的量分数为0.5mol÷(1mol+1mol)= 25%;该反应的化学平衡常数K=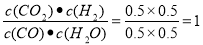 ;(2)向该平衡体系中通入1.0mol水蒸气,假设反应消耗的CO为x,则消耗的H2O也是x,达到平衡时产生CO2、H2的物质的量也都是x,则达到新的平衡状态时,各种物质的物质的量是CO :(1-x)mol; H2O :(2-x)mol;由于温度不变,所以化学平衡常数不变。(1-x)×(2-x)=x2.解得x=2/3mol,所以平衡时水蒸气的物质的量为(2-x)mol=(2—2/3)mol=1.33mol ;则CO的转化率为(2/3mol)÷1.0mol=66.7%。
;(2)向该平衡体系中通入1.0mol水蒸气,假设反应消耗的CO为x,则消耗的H2O也是x,达到平衡时产生CO2、H2的物质的量也都是x,则达到新的平衡状态时,各种物质的物质的量是CO :(1-x)mol; H2O :(2-x)mol;由于温度不变,所以化学平衡常数不变。(1-x)×(2-x)=x2.解得x=2/3mol,所以平衡时水蒸气的物质的量为(2-x)mol=(2—2/3)mol=1.33mol ;则CO的转化率为(2/3mol)÷1.0mol=66.7%。
考点:考查化学平衡常数的计算、物质的平衡转化率的计算的知识。

练习册系列答案
相关题目
 2HI(g) ,已知H2和I2的起始浓度均为0.1 mol·L-1时,达平衡时HI浓度为0.16 mol·L-1。若H2和I2的起始浓度均变为0.2 mol·L-1,则平衡时H2的浓度(mol·L-1)是
2HI(g) ,已知H2和I2的起始浓度均为0.1 mol·L-1时,达平衡时HI浓度为0.16 mol·L-1。若H2和I2的起始浓度均变为0.2 mol·L-1,则平衡时H2的浓度(mol·L-1)是