题目内容
5.下列关于铁及其化合物的说法中正确的是( )| A. | 赤铁矿的主要成分是Fe3O4 | |
| B. | 铁与水蒸气在高温下反应得产物为Fe2O3和H2 | |
| C. | 在空气中灼烧Fe(OH)3最终得到Fe2O3 | |
| D. | Cl2与过量的铁粉反应生成FeCl2 |
分析 A.Fe3O4为黑色固体;
B.反应生成四氧化三铁;
C.灼烧Fe(OH)3最终得到Fe2O3;
D.Cl2与过量的铁粉反应生成FeCl3.
解答 解:A.Fe3O4是一种黑色固体,俗称磁铁矿,赤铁矿的主要成分是Fe2O3,故A错误;
B.铁与水蒸气在高温下的反应产物为Fe3O4和H2,故B错误;
C.灼烧Fe(OH)3最终得到Fe2O3,故C正确;
D.因为氯气具有强氧化性,并且氯气与铁反应不在溶液中进行,所以Cl2与过量的铁粉反应生成FeCl3,故D错误;
故选C.
点评 本题考查铁及其化合物的性质,为高频考点,把握常见铁化合物的性质及发生的氧化还原反应为解答的关键,侧重分析应用能力的考查,题目难度不大.

练习册系列答案
相关题目
16.用硫酸铁电化浸出黄铜矿精矿工艺中,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+═Cu2++5Fe2++2S.下列说法正确的是( )
| A. | 反应中硫元素被氧化,所有铁元素均被还原 | |
| B. | 当转移1mol电子时,46 g CuFeS2参加反应 | |
| C. | 氧化产物是S,还原产物是Cu2+和Fe2+ | |
| D. | 还原剂是S2-,氧化剂是Fe3+ |
10.Fe、FeO、Fe3O4的混合物中,加入100mL 2mol/L的盐酸,恰好使混合物完全溶解,放出44.8mL(标准状况)的气体,所得溶液中加入KSCN溶液无血红色出现,若用足量的CO在高温下还原相同质量的此混合物,能得到铁( )
| A. | 2.8 g | B. | 5.6 g | C. | 11.2 g | D. | 无法确定 |
8.为了测定酸碱反应的中和热,计算时至少需要的数据是( )
①酸的浓度和体积;
②碱的浓度和体积;
③比热容;
④反应后溶液的质量;
⑤生成水的质量;
⑥前后温度的变化;
⑦操作所需时间.
①酸的浓度和体积;
②碱的浓度和体积;
③比热容;
④反应后溶液的质量;
⑤生成水的质量;
⑥前后温度的变化;
⑦操作所需时间.
| A. | ①②④⑥ | B. | ③④⑤⑥ | C. | ①③④⑤ | D. | 全部 |
 向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
向20mL某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示: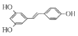 )具有预防心血管疾病的作用,其一种合成路线如图:
)具有预防心血管疾病的作用,其一种合成路线如图: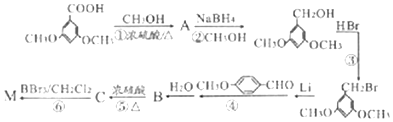
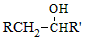
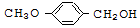 $\stackrel{BBr_{3}/CH_{2}Cl_{2}}{→}$
$\stackrel{BBr_{3}/CH_{2}Cl_{2}}{→}$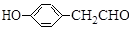 回答下列问题:
回答下列问题: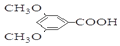 核磁共振氢谱中不同化学环境的氢原子个数比为6:1:2:1.
核磁共振氢谱中不同化学环境的氢原子个数比为6:1:2:1. .
. .
.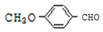 有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有3种.
有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有3种.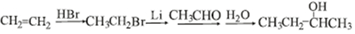 .
.
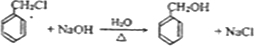 .
. .
.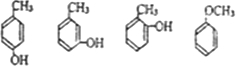 写出其中一种.
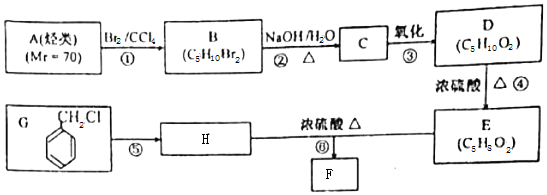
写出其中一种.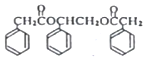 .(在方框内写中间体的结构简式,在“→”上方或下方写反应所需条件或试剂)
.(在方框内写中间体的结构简式,在“→”上方或下方写反应所需条件或试剂)