题目内容
奶粉行业的“911事件”将三聚氰胺引入公众视野,工业上可用尿素为原料,在一定条件下合成三聚氰胺:6CO(NH2)2→6NH3+3CO2+C3H6N6,对C3H6N6说法正确的是( )
| A、摩尔质量为126 |
| B、相对分子质量为126g?mol-1 |
| C、每个C3H6N6分子含3个N2分子 |
| D、0.1 mol C3H6N6含碳原子数为1.806×1023 |
考点:物质的量的相关计算
专题:计算题
分析:A.根据摩尔质量的单位进行判断;
B.相对分子质量没有单位;
C.根据三聚氰胺(C3H6N6)为化合物进行判断;
D.根据三聚氰胺(C3H6N6)的分子组成计算出含有碳原子的物质的量及数目.
B.相对分子质量没有单位;
C.根据三聚氰胺(C3H6N6)为化合物进行判断;
D.根据三聚氰胺(C3H6N6)的分子组成计算出含有碳原子的物质的量及数目.
解答:
解:A.三聚氰胺(C3H6N6)的摩尔质量为126 g?mol-1,故A错误;
B.三聚氰胺(C3H6N6)的相对分子质量为126,故B错误;
C.每个C3H6N6分子中含有6个氮原子,不存在N2分子,故C错误;
D.0.1NA个C3H6N6分子中含有0.3molC,含碳原子数为1.806×1023,故D正确;
故选D.
B.三聚氰胺(C3H6N6)的相对分子质量为126,故B错误;
C.每个C3H6N6分子中含有6个氮原子,不存在N2分子,故C错误;
D.0.1NA个C3H6N6分子中含有0.3molC,含碳原子数为1.806×1023,故D正确;
故选D.
点评:本题考查摩尔质量、阿伏伽德罗常数、相对分子量等知识,比较基础,注意对基础知识的理解掌握.

练习册系列答案
相关题目
根据现行元素周期表的排布规律,如果第七周期排满,下列预测正确的是( )
| A、第七周期共有50种元素 |
| B、第七周期最后一种元素不与任何物质发生反应 |
| C、第七周期ⅦA族元素的原子在化学反应中可以得到1个电子 |
| D、第七周期任何一种元素的原子最外层上不超过8个电子 |
下列离子方程式中正确的是( )
| A、向硫酸铜蓝色溶液中加入BaCl2溶液:Ba2++SO42-═BaSO4↓ | ||||
| B、碳酸氢钙溶液跟盐酸反应:Ca(HCO3)2+2H+=Ca2++2H2O+2CO2↑ | ||||
| C、锌与盐酸的反应:Zn+2H++2Cl-═Zn2++2Cl-+H2↑ | ||||
D、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O
|
在不同条件下分别测得反应2SO2+O2?2SO3的化学反应速率,其中表示该反应进行最快的是( )
| A、v(SO2)=4 mol?L-1?min-1 |
| B、v (O2)=3 mol?L-1?min-1 |
| C、v (SO3)=0.1 mol?L-1?s-1 |
| D、v (O2)=0.1mol?L-1?s-1 |
下列实验操作不正确的是( )
| A、蒸发结晶时,应将蒸发皿中的NaCl溶液全部蒸干才停止加热 |
| B、蒸馏实验中,要在烧瓶中加入沸石或碎瓷片,以防止液体暴沸 |
| C、用托盘天平称量药品时,将砝码置于天平右盘 |
| D、用浓硫酸配制一定物质的量浓度的稀硫酸时,应冷却至室温再转移到容量瓶中 |
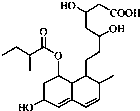 普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )| A、能与FeCl3溶液发生显色反应 |
| B、能使酸性KMnO4溶液褪色 |
| C、能发生加成、取代、消去反应 |
| D、1mol该物质最多可与1molNaOH反应 |
下列离子方程式书写正确的是( )
| A、铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ | ||
| B、氢氧化钡与硫酸铜溶液混合:2OH-+Cu2+=Cu(OH)2↓ | ||
C、过量NaHCO3溶液和少量Ba(OH)2反应:2HCO
| ||
| D、石灰乳和盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
短周期元素X、Y、Z所在的周期数依次增大,它们的原子序数之和为20,且Y2-与Z+核外电子层的结构相同.下列化合物中同时存在离子键和非极性共价键的是( )
| A、Z2Y |
| B、X2Y2 |
| C、ZYX |
| D、Z2Y2 |
下面关于电解质的叙述中错误的是( )
| A、在水溶液中和熔融状态下均不导电的化合物叫非电解质 |
| B、电解质、非电解质都指化合物而言,单质不属于此范畴 |
| C、BaSO4在水中溶解度很小,故BaSO4是非电解质 |
| D、纯水的导电性很差,所以水不是电解质 |