��Ŀ����
��12�֣�
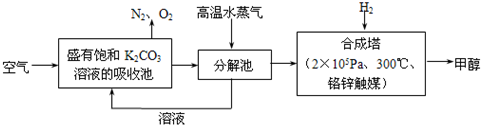
Ϊ��С������CO2�Ի�����Ӱ�죬�п�ѧ���������ɫ���ɡ����롣���Ȱѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ��������ʹ֮��Ϊ������ȼ�ϼ״�������ɫ���ɡ����뼼���������£�

��1��д���ֽ���з�Ӧ�Ļ�ѧ����ʽ ��
��2���ںϳ����У�����4��4kg CO2������H2��ȫ��Ӧ���ɷų�����4947 kJ��д���ϳ����з�Ӧ���Ȼ�ѧ����ʽ ��
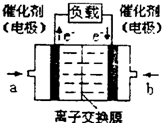
��3��д������������Ϊ����ʵļ״�ȼ�ϵ�صĸ�����Ӧʽ ��
������ת��Ϊ molʱ���μӷ�Ӧ�������������6��72L����״���£���
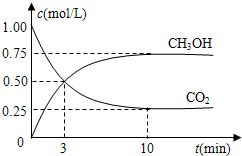
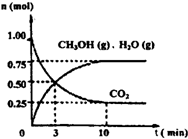
��4�������Ϊl L���ܱ������У�����1mol CO2��3molH2��500��C�·�����Ӧ���й����ʵ�Ũ����ʱ�ʱ仯����ͼ��ʾ��

�ٴӷ�Ӧ��ʼ��ƽ�⣬H2��ƽ����Ӧ����v��H2��= ��
���������������䣬ֻ���¶���ߵ�800��C���ٴδ�ƽ��ʱ��n��CH3OH��/n��CO2����ֵ �����������С�����䡱����
��1��2KHCO3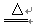 K2CO3+H2O+CO2��
K2CO3+H2O+CO2��
��2��CO2��g��+3H2��g��=CH3OH��g��+H2O��g�� ��H=-49.47kJ/mol
��3��CH3OH+8OH��6e-=CO2-3+6H2O�� 1.2mol
��4����0.225mol/��L��min�����ڼ�С
��������

 ��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���
��2012?������ģ����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������ȫ������ձ����ӣ�Ϊ��С������CO2�Ի�����Ӱ�죬һ����������������������ŷ�������һ�����ѧ�Ҽ�ǿ�˶�CO2�������õ��о���