题目内容
2.已知NH4++AlO2-+2H2O═Al(OH)3↓+NH3•H2O,向含有等物质的量的NH4+、Al3+、H+混合溶液中,慢慢滴加NaOH溶液直至过量,并不断搅拌,发生以下离子反应:①H++OH-═H2O ②Al(OH)3+OH-═AlO2-+2H2O
③Al3++3OH-═Al(OH)3↓ ④NH4++OH-═NH3•H2O
先后顺序正确的是( )
| A. | ①→④→③→② | B. | ①→③→②→④ | C. | ①→②→③→④ | D. | ①→③→④→② |
分析 由于Al(OH)3和NH3•H2O都与氢离子反应,但氢氧根离子先与氢离子反应,由于NH4++AlO2-+2H2O=Al(OH)3↓+NH3•H2O可知,氢氧根离子与铝离子反应,然后与铵根离子反应,最后与Al(OH)3反应.
解答 解:由于Al(OH)3和NH3•H2O都与氢离子反应,氢氧根离子先与氢离子反应①H++OH-=H2O,由于NH4++AlO2-+2H2O=Al(OH)3↓+NH3•H2O,氢氧根离子再与铝离子反应③Al3++3OH-=Al(OH)3↓,然后与铵根离子反应④NH4++OH-=NH3•H2O,最后与Al(OH)3反应②Al(OH)3+OH-=AlO2-+2H2O.
故选D.
点评 本题考查离子反应,为高频考点,把握习题中的信息及离子反应的先后顺序为解答的关键,侧重分析与应用能力的考查,注意Al(OH)3不能溶解在弱碱中、中和优先于沉淀的溶解,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.用 NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 17 g-OH与 17 g OH-所含电子数均为 10NA | |
| B. | 标准状况下,22.4 L 己烷中含共价键数目为 19NA | |
| C. | 常温常压下,28 g C2H4和 C3H6的混合气体中含有的原子数为 6NA | |
| D. | 1 mol 苯分子中含有的碳碳双键数为 3NA |
13.室温下,下列溶液的说法不正确的是( )
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
| pH | 11 | 11 | 3 | 3 |
| A. | 水的电离程度:①=②=③=④ | |
| B. | 分别加水稀释10倍,溶液的pH:①>②>③>④ | |
| C. | ①、③两溶液等体积混合:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | V1L②溶液与V2 L③溶液混合,若混合溶液pH=4,则V1:V2=9:11(忽略溶液体积变化) |
10.相对分子质量在300以下的某脂肪酸1.0g与2.7g碘可完全加成,也可被0.2gKOH所中和,则该脂肪酸的相对分子质量的准确值是( )
| A. | 278 | B. | 280 | C. | 282 | D. | 无法确定 |
1.下列有机物命名正确的是( )
| A. | 3,3-二甲基丁烷 | B. | 3-甲基-2-乙基戊烷 | ||
| C. | 2,3-二甲基戊烯 | D. | 3-甲基-1-戊炔 |
2.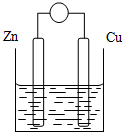 原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
填表:
【注意】①电解质溶液的pH增大
②在同一个电池中两极反应时,“失去电子数”与“得到电子数”要相同.
(3)原电池工作时电子、离子运动方向.
①外电路(导线):电子从负极经导线流向正极
②原电池内电解质溶液中:阴离子流向负极,阳离子流向正极.
 原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.
原电池是将化学能转变成电能的装置.原电池结构示意图(以Zn-Cu-稀H2SO4原电池为例)铜片和锌片作电极,稀硫酸做电解质溶液.填表:
| 电极 | 电极材料 | 电极反应式 | 反应类型 |
| 正极 | |||
| 负极 | |||
| 总反应式 | |||
②在同一个电池中两极反应时,“失去电子数”与“得到电子数”要相同.
(3)原电池工作时电子、离子运动方向.
①外电路(导线):电子从负极经导线流向正极
②原电池内电解质溶液中:阴离子流向负极,阳离子流向正极.
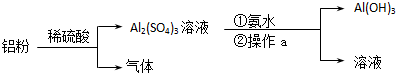
 ;
; ;
; ;
;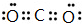 ;
;
 .
.