题目内容
12.铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )①铊是易导电的银白色金属
②Tl(OH)3是两性氢氧化物
③Tl3+的氧化能力比Al3+强
④单质能和稀硝酸反应生成硝酸盐.
| A. | ①④ | B. | ②③ | C. | ① | D. | ④ |
分析 铊与铝是同族元素,则具有金属的共性,化合物中元素的化合价为+3价,且金属性Tl>Al,以此来解答.
解答 解:①铊与铝是同族元素,属于金属元素,则是银白色、质软的金属,故①正确;
②同主族从上到下金属性在增强,Al(OH)3是两性氢氧化物,但Tl(OH)3是碱性氢氧化物,故②错误;
③金属性Tl>Al,则Tl3+的氧化能力比Al3+弱,故③错误;
④Tl较活泼,则该金属能与硝酸反应生成硝酸盐,故④正确;
故选B.
点评 本题考查同主族元素的性质,明确元素周期律是解答本题的关键,注意性质的相似性和递变性来解答即可,难度不大.

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
3.一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通甲烷和氧气,其电池反应为:
X极:CH4+10OH--8e-=CO32-+7H2O
Y极:O2+4e-+2H2O=4OH-
下列关于此燃料电池的有关说法中错误的是( )
X极:CH4+10OH--8e-=CO32-+7H2O
Y极:O2+4e-+2H2O=4OH-
下列关于此燃料电池的有关说法中错误的是( )
| A. | 通过甲烷的电极(X)为电池的负极,通过氧气的电极(Y)为电池正极 | |
| B. | 放电一段时间后,电解质溶液中KOH的物质的量不改变 | |
| C. | 在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移 | |
| D. | 放电时,通过甲烷的一极附近的pH降低 |
20.下列说法正确的是( )
| A. | 氨水中的溶质是NH3•H2O | |
| B. | NH3有碱性,所以能使湿润的红色石蕊试纸变蓝色 | |
| C. | 所有的铵盐都易溶于水,且受热易分解 | |
| D. | 常温下,浓硫酸、浓硝酸与铁、铝均不反应,所以可用铁制的容器来储存和运输 |
7.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有跟氖原子相同的电子层结构,则正确的是( )
| A. | 原子半径 A>B>D>C | |
| B. | 原子序数 d>c>b>a | |
| C. | 离子半径 C3->D->B+>A2+ | |
| D. | 原子结构的最外层电子数目 A>B>D>C |
17.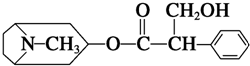 我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示:
我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示:
下列有关金丝桃素的说法:
①属于烃的衍生物,燃烧只产生CO2和H2O
②可以发生取代、加成、酯化、消去等反应
③分子式为C17H23O3N,苯环上的一氯取代物有3种
④1mol该物质最多能和4mol H2发生加成反应
其中正确的是( )
 我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示:
我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构简式如图所示:下列有关金丝桃素的说法:
①属于烃的衍生物,燃烧只产生CO2和H2O
②可以发生取代、加成、酯化、消去等反应
③分子式为C17H23O3N,苯环上的一氯取代物有3种
④1mol该物质最多能和4mol H2发生加成反应
其中正确的是( )
| A. | ①和④ | B. | ②和④ | C. | ②和③ | D. | ①和③ |
4.向一定量的FeO、Fe、Fe3O4的混合物中加入100mL 1mol•L-1的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体,在所得溶液中经检验无Fe3+.若用足量的CO在高温下还原相同质量的此混合物,能得到铁的质量是( )
| A. | 11.2g | B. | 5.6g | C. | 2.8g | D. | 无法计算 |
1.下列关于多电子原子的核外电子运动规律的叙述正确的是( )
①核外电子是分层运动的 ②所有电子在同一区域里运动 ③能量高的电子在离核近的区域里运动 ④能量低的电子在离核近的区域里运动.
①核外电子是分层运动的 ②所有电子在同一区域里运动 ③能量高的电子在离核近的区域里运动 ④能量低的电子在离核近的区域里运动.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
2.下列数值关系中不正确的是( )
| A. | 原子序数=原子核内质子数 | |
| B. | 元素的种数=原子种数 | |
| C. | 元素周期表中主族序数=原子的最外层电子数 | |
| D. | 元素周期表中周期数=原子的电子层数 |