题目内容
(1)混合动力汽车因具有能量利用率高(95%以上)、节省汽油、发动机噪音低和几乎没有尾气污染等优良性能,受到越来越多的关注,某种混合动力汽车的动力系统由“1.3L汽油机+5速手动变速器+10kW电机+144V镍氢电池”组成。
①汽油机的燃料之一是乙醇,1g乙醇完全燃烧放出29.7kJ热量,写出乙醇燃烧的热化学方程式___________________________________。
②镍氢电泄的使用可减少重金属离子污染,它采用储氢金属作为负极,碱液(主要是KOH)作为电解液,镍氢电池充电时发生反应:Ni(OH)2=== Ni(OH)+1/2H2。其放电时正极电极反应式为__________________________________。
③常温下,浓度同为0.1mol·L-l的NaHCO3溶液和Na2CO3 溶液pH 值都大于7 ,两者中_______ pH更大,其原因是:___________________________________。
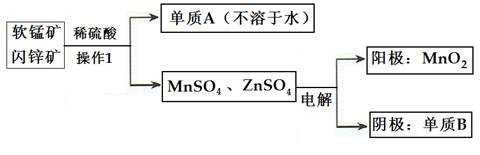
(2)二氧化锰、锌是制造干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:
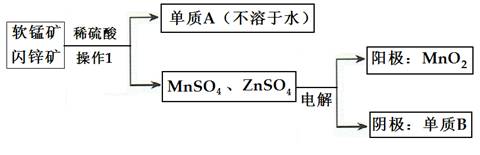
①操作1的名称为___________,单质A为____________,单质B为______________。
②上述电解过程中,当阴极生成6.5gB时阳极生成MnO2质量为_________________。
③利用铝热反应原理,可从软锰矿中提取单质锰,写出其化学反应式:__________________________________________
(l)①CH3CH2OH(l)+3O2(g)=== 2CO2(g)+3H2O(l);△H= -1366.2kJ/m
②NiO(OH)+ H2O+e===Ni(OH)2+OH-(3分)
③Na2CO3溶液(2分) 由HCO3-电离出H+和CO32- 比由H2CO3电离出H+和CO32-更难,即Na2CO3是更弱酸的盐,其水解程度更大,碱性更强,pH值更大。(2分)
⑵①过滤 S Zn (6分)②8.7g(2分)③![]() (2分)
(2分)

(18分)(1)混合动力汽车因具有能量利用率高(95%以上)、节省汽油、发动机噪音低和几乎没有尾气污染等优良性能,受到越来越多的关注,某种混合动力汽车的动力系统由“1.3L汽油机+5速手动变速器+10kw电机+144v镍氢电池”组成。
①汽油机的燃烧之一是乙醇,1克乙醇完全燃烧放出29.7kJ热量,写出乙醇燃烧的热化学方程式 。
②镍氢电池的使用可减少重金属离子污染,其采用储氢金属作为负极,碱液(主要是KOH)作为电解液,镍氢电池充电时发生反应:Ni(OH)2 === NiO(OH)+ H2。其放电时的正极电极反应式为 。
③常温下,浓度同为0.1mol/L的NaHCO3溶液和Na2CO3溶液pH值都大于7,两者中 pH更大,其原因是: 。
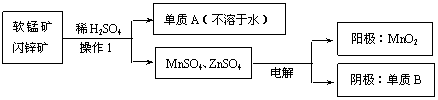
(2)二氧化锰、锌是制造干电池的重要原料,工业上用软锰矿(含MnO2)和闪锌矿(含ZnS)联合生产二氧化锰、锌的工艺如下:
 |
![]()
![]()
![]()
![]()
①操作1的名称为 ,单质A为 ,单质A为 。
![]()
②上述电解过程中,当阴极生成6.5g B时阳极生成的MnO2质量为 。
③利用铝热反应原理,可从软锰矿中提取出单质锰,写出其反应方程式: 。