题目内容
16.下列装置(加持装置略去)能达到试验目的是( )| 选项 | A | B | C | D |
| 装置 |  |  |  |  |
| 实验目的 | 比较非金属性:N>C>Si | 制备并收集乙酸乙酯 | 除去Ca(OH)2中的NH4Cl | 验证HCl的溶解性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.硝酸具有挥发性,挥发出的硝酸能够与硅酸钠溶液反应生成硅酸;
B.收集乙酸乙酯的导管不能插入碳酸氢钠溶液,否则易发生倒吸现象;
C.加热条件下氢氧化钙与氯化铵发生反应生成氯化钙和氨气;
D.滴加水后,根据气球是否膨胀可判断氯化氢的溶解性.
解答 解:A.硝酸易挥发,应除掉二氧化碳中的硝酸,再与硅酸钠反应,否则干扰了检验结果,故A错误;
B.制备乙酸乙酯时,收集乙酸乙酯的导致不能深入饱和碳酸氢钠溶液中,否则挥发出的乙酸、乙醇易溶于水,会发生倒吸现象,故B错误;
C.由于Ca(OH)2与NH4Cl在加热条件下反应生成氨气和氯化钙,无法通过加热除去Ca(OH)2中的NH4Cl,故C错误;
D.HCl溶于水后,烧杯中气体压强小于大气球,气球膨胀,从而可证明HCl的溶解性,故D正确;
故选D.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及非金属性强弱判断、乙酸乙酯的制备、物质除杂等知识,注意掌握常见化学实验基本操作方法,明确物质分离与除杂方法,试题培养了学生的化学实验能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.范德华力为a kJ•mol-1,化学键为b kJ•mol-1,氢键为c kJ•mol-1,则a、b、c的大小关系是( )
| A. | b>c>a | B. | b>a>c | C. | c>b>a | D. | a>b>c |
7.氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料.
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3 该可逆反应达到平衡的标志是BCE.
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间而变化
E.a mol N≡N键断裂的同时,有6a mol N-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(2)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如表:
则从反应开始到25min时,以N2表示的平均反应速率=0.01 mol/(L•min);
该温度下平衡常数K=2.37.
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3 该可逆反应达到平衡的标志是BCE.
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间而变化
E.a mol N≡N键断裂的同时,有6a mol N-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(2)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如表:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
该温度下平衡常数K=2.37.
4.(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、环形玻璃搅拌棒、量筒.
(2)量取反应物时,取50mL 0.50mol•L-1的盐酸,还需加入的试剂是B.
A.50mL 0.50mol•L-1 NaOH溶液 B.50mL 0.55mol•L-1 NaOH溶液
C.1.0g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得的中和热数值偏小(填偏大、偏小、无影响)
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如表所示.
①设充分反应后溶液的比热容c=4.18J/(g•℃),忽略实验仪器的比热容及溶液体积的变化,则△H1=-56.8kJ/mol;△H2=-52.7kJ/mol.(已知溶液密度 均为1g/cm3)
②△H1≠△H2原因是NaOH是强碱,NH3•H2O是弱碱电离吸热.
(2)量取反应物时,取50mL 0.50mol•L-1的盐酸,还需加入的试剂是B.
A.50mL 0.50mol•L-1 NaOH溶液 B.50mL 0.55mol•L-1 NaOH溶液
C.1.0g NaOH固体
(3)实验时大烧杯上若不盖硬纸板,求得的中和热数值偏小(填偏大、偏小、无影响)
(4)由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如表所示.
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ•mol-1 |
| A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL | 13.0 | 19.8℃ | △H1 |
| B.1.0mol/L HCl溶液50mL、1.1mol/L NH3•H2O溶液50mL | 13.0 | 19.3℃ | △H2 |
②△H1≠△H2原因是NaOH是强碱,NH3•H2O是弱碱电离吸热.
11.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.
(1)Fe还原水体中NO3-的反应原理如图1所示.

②作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
pH=4.5时,NO3-的去除率低.其原因是FeO(OH)不导电,阻碍电子转移.
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如右图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率.
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.pH=4.5(其他条件相同)
(1)Fe还原水体中NO3-的反应原理如图1所示.

②作负极的物质是铁.
②正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 |  |  |
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3-;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如右图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率.
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.pH=4.5(其他条件相同)
1.某有机化合物结构简式如图,下列有关它的性质的叙述中,正确的是( )


| A. | 有弱酸性,与Na2CO3、NaHCO3溶液均能反应 | |
| B. | 在一定条件下,1 mol该物质最多能与3 mol NaOH完全反应 | |
| C. | 在一定条件下,该物质可以发生取代、加成、水解、消去反应 | |
| D. | 该有机物分子中所有碳原子可能共平面 |
8.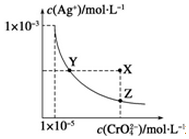 在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )
在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )
 在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )
在t℃时,Ag2CrO4(橘红色)在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgBr的Ksp=5.0×10-13,下列说法错误的是( )| A. | t℃时,Ag2CrO4的Ksp为1×10-8 | |
| B. | 在饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点 | |
| C. | 一定温度下Y点和Z点时Ag2CrO4的Ksp相等 | |
| D. | 在t℃时,Ag2CrO4(s)+2Br-(aq)?2AgBr(s)+CrO42-(aq)平衡常数K=4.0×1010 |
6.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子最外层比次外层多3个电子;Y、Z均为金属,Y是同周期中原子半径最大的元素,Z的简单离子半径在同周期元素中最小;W的最高价氧化物在无机含氧酸中酸性最强.下列说法正确的是( )
| A. | X的气态氢化物的热稳定性比O(氧)的强 | |
| B. | 元素Z、W的简单离子具有相同的电子层结构 | |
| C. | Y、Z、W的最高价氧化物对应的水化物之间能相互反应 | |
| D. | 等质量的Y和Z单质分别与足量稀盐酸反应,前者产生的氢气多 |
 图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色反应均为黄色.请填写下列空白:
图示中,A为一种常见的单质,B、C、D、E是含有A元素的常见化合物,它们的焰色反应均为黄色.请填写下列空白: