题目内容
下列说法正确的是( )
| A、氧化性弱的物质还原性定强 |
| B、在反应中失电子多的物质一般比少的物质的还原性要强 |
| C、物质所含元素化合价升高的反应是还原反应 |
| D、氧化反应和还原反应是同时发生的 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.氧化性弱的还原性不一定强;
B.失去电子的多少与还原性无关;
C.所含元素化合价升高,则失去电子被氧化;
D.氧化与还原反应共存于同一个反应中.
B.失去电子的多少与还原性无关;
C.所含元素化合价升高,则失去电子被氧化;
D.氧化与还原反应共存于同一个反应中.
解答:
解:A.氧化性弱的还原性不一定强,如碳酸、二氧化硅等,故A错误;
B.失去电子的多少与还原性无关,还原性与失去电子的难易程度有关,故B错误;
C.所含元素化合价升高,则失去电子被氧化,发生氧化反应,故C错误;
D.氧化与还原反应共存于同一个反应中,则氧化反应和还原反应是同时发生的,故D正确;
故选D.
B.失去电子的多少与还原性无关,还原性与失去电子的难易程度有关,故B错误;
C.所含元素化合价升高,则失去电子被氧化,发生氧化反应,故C错误;
D.氧化与还原反应共存于同一个反应中,则氧化反应和还原反应是同时发生的,故D正确;
故选D.
点评:本题综合考查氧化还原反应知识,为高考常见题型和高频考点,侧重于学生的分析能力和计算能力的考查,注意从实例的角度分析,题目难度不大.

练习册系列答案
相关题目
下列不能用于实验室制取NH3的是( )
| A、Ca(OH)2固体与NH4Cl晶体混合加热 |
| B、分解NH4Cl晶体 |
| C、分解NH4HCO3晶体 |
| D、将浓氨水加入到锥形瓶中的CaO固体上 |
BF3熔点和沸点都比较低,下列有关叙述不正确的是( )
| A、BF3分子中键与键之间的夹角为120° |
| B、BF3中心原子采用sp3杂化 |
| C、BF3分子呈正三角形,中心原子无孤对电子 |
| D、BF3分子立体结构与CO32-相同 |
用R代表短周期元素,R原子最外层的p能级上的未成对电子只有2个.下列关于R的描述中正确的是( )
| A、R的氧化物都能溶于水 |
| B、R都是非金属元素 |
| C、R的氧化物都能与NaOH反应 |
| D、R的最高价氧化物对应的水化物都是H2RO3 |
下列说法不正确的是( )
| A、水结成冰体积膨胀的事实与氢键有关 |
| B、在水中的溶解度:C2H5OH>CH3CH2CH2CH2OH |
| C、CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 |
| D、利用相似相溶原理不能解释:I2微溶于水,易溶于CCl4;HCl易溶于水 |
下列叙述中,不正确的是( )
①原子晶体中只含有极性键
②金属在常温时都以晶体形式存在
③离子晶体一定含离子键,也可能有共价键
④分子晶体中一定有分子间作用力,有的还可能有氢键.
①原子晶体中只含有极性键
②金属在常温时都以晶体形式存在
③离子晶体一定含离子键,也可能有共价键
④分子晶体中一定有分子间作用力,有的还可能有氢键.
| A、①④ | B、②③ | C、①② | D、①③ |
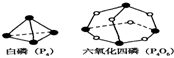 化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ?mol-1)P-P:198 P-O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为( )
化学反应可视为旧键的断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(KJ?mol-1)P-P:198 P-O:360 O=O:498 则反应P4(白磷)+3O2→P4O6 的反应热△H为( )| A、+1638KJ?mol-1 |
| B、-1638KJ?mol-1 |
| C、+126KJ?mol-1 |
| D、-126KJ?mol-1 |
设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是( )
| A、1 mol NH3所含有的原子数为NA 个 |
| B、常温常压下,22.4 L氧气所含的原子数为2NA个 |
| C、常温常压下,48 g O3所含的氧原子数为3NA 个 |
| D、1 L 0.1 mol/LNaCl溶液中所含的Na+为NA个 |