题目内容
5.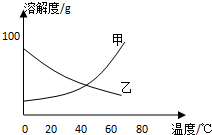 甲、乙两种固体纯净物的溶解度曲线如图所示.在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里.下列说法正确的是( )
甲、乙两种固体纯净物的溶解度曲线如图所示.在常温下,先在两支试管里分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里.下列说法正确的是( )| A. | 乙溶液中溶质的质量分数增大 | B. | 装甲溶液的试管中剩余的固体减少 | ||
| C. | 试管里甲、乙物质的溶解度都增大 | D. | 两支试管里剩余的固体都增多 |
分析 常温下物质的饱和溶液(试管底部均有未溶解的固体)放进盛有冰水的烧杯里,操作的目的是对饱和溶液进行降温;根据溶解度曲线得知,甲物质的溶解度随温度降低而减小,乙物质的溶解度随温度降低而增大,据此分析解答.
解答 解:A.乙物质的溶解度随温度降低物质的溶解度变大,所以放入冰水后,随温度降低乙物质的溶解度变大,试管底部固体物质乙继续溶解,溶液中溶质质量增加,所以乙溶液中溶质的质量分数增大,故A正确;
B.甲物质的溶解度曲线表明,温度降低物质的溶解度减小,所以,放入冰水后,随温度降低甲物质的溶解度变小,试管内饱和溶液析出晶体,剩余固体物质甲增加,故B错误;
C.固体物质的溶解度受温度影响,根据溶解度曲线得知,甲物质的溶解度随温度降低而减小,乙物质的溶解度随温度降低而增大,故C错误;
D.综合A、B两项的分析可得,盛甲物质的试管内固体物质增加,而盛乙物质的试管内固体物质减少,故D错误.
故选A.
点评 本题考查固体溶解度曲线以及固体溶解度的影响因素,注意对相关概念的准确理解,难度中等.

练习册系列答案
相关题目
15.锰的化合物种类较多,也大多具有广泛的用途.
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性.某化学兴趣小组通过实验探究Mn O2的性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是D.
A.把Mn02固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把Mn O2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2S03溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeS04溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸.现象记录如下:
①从以上实验中,我们可以得出的结论是酸性越强,MnO2氧化性越强.
②写出C试管中发生反应的离子方程式:2I-+MnO2+4H+═I2+Mn2++2H2O.
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机.MnFe2O4的制备工艺流程如图:

已知Fe3+、Mn2+沉淀的pH为下表所示.
①步骤一中投入原料Fe(NO3)3和Mn(N03)2的物质的量之比理论上应为2:1.
②步骤二中需控制pH的范围是PH≥10.4.
③步骤三中是否洗涤干净的判断方法是取最后一次洗涤液,做焰色反应,通过蓝色的钴玻璃观察无紫色出现,说明不含钾离子,洗涤干净.
I.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性.某化学兴趣小组通过实验探究Mn O2的性质.
(1)该小组设计了如下4个方案以验证MnO2的氧化性,可行的是D.
A.把Mn02固体加入到稀盐酸中,观察是否有黄绿色气体生成
B.把Mn O2固体加入到H2O2溶液中,观察是否有气泡产生
C.Na2S03溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
D.FeS04溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
(2)为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL 0.2mol/L NaOH溶液、1mL水、1mL 0.1mol/L硫酸.现象记录如下:
| 试管编号 | 实验现象 |
| A | 溶液不变色 |
| B | 溶液缓慢变浅棕褐色 |
| C | 溶液迅速变棕褐色 |
②写出C试管中发生反应的离子方程式:2I-+MnO2+4H+═I2+Mn2++2H2O.
Ⅱ,铁酸锰( MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机.MnFe2O4的制备工艺流程如图:

已知Fe3+、Mn2+沉淀的pH为下表所示.
| 开始沉淀 | 完全沉淀 | |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
②步骤二中需控制pH的范围是PH≥10.4.
③步骤三中是否洗涤干净的判断方法是取最后一次洗涤液,做焰色反应,通过蓝色的钴玻璃观察无紫色出现,说明不含钾离子,洗涤干净.
16.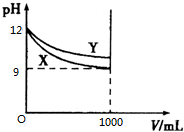 常温下pH=12的X、Y两种碱溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示.下列说法正确的是( )
常温下pH=12的X、Y两种碱溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示.下列说法正确的是( )
 常温下pH=12的X、Y两种碱溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示.下列说法正确的是( )
常温下pH=12的X、Y两种碱溶液各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示.下列说法正确的是( )| A. | X是弱碱,Y是强碱 | |
| B. | X、Y两种溶液稀释前溶质的物质的量浓度相等 | |
| C. | 两种溶液稀释后恢复至原温度,溶液中c(H+)与c(OH-)之比都变大 | |
| D. | 两种溶液稀释后恢复至原温度,溶液中c(H+)与c(OH-)的乘积都变小 |
13.下列关于实验说法正确是( )
| A. | 氯气可以使湿润的红色布条褪色,所以氯气具有漂白性 | |
| B. | 在配制一定浓度的溶液时未冷却溶液直接将溶液转移至容量瓶中,则浓度偏高 | |
| C. | 因为KNO3的溶解度很大,所以可以用重结晶法除去KNO3中的NaCL杂质 | |
| D. | 向饱和FeCl3溶液中逐滴滴加沸水可以制备Fe(OH)3胶体 |
20.能用离子方程式OH+H+=H2O表示的反应是( )
| A. | 稀盐酸和稀氨水反应 | B. | 稀硫酸和烧碱溶液反应 | ||
| C. | 稀硫酸和氢氧化铜反应 | D. | 稀硫酸和氢氧化钡溶液反应 |
14.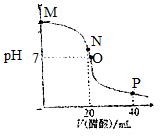 常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
 常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )
常温下,向20.0mL 0.10mol•L-1的NaOH溶液中逐滴加入0.10mol•L-1的醋酸溶液,溶液pH随醋酸溶液体积的变化如图所示.下列说法正确的是( )| A. | N点处恰好完全反应,c(CH3COO-)=c(CH3COOH) | |
| B. | O点处显中性,c(CH3COO-)=c(Na+)=c(H+)=c(OH-) | |
| C. | M点到O点过程中,可能出现c(CH3COO-)>c(Na+) | |
| D. | P点处显酸性,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
15.用NA表示阿伏加德常数,以下的说法正确的是( )
| A. | 精炼铜时,阳极有1mol物质放电,阴极一定生成NA个铜原子 | |
| B. | 在标准状况下,NA个SO3 分子的质量是80g,其体积就为80/ρ (ρ为SO3的密度) | |
| C. | 1molNaHSO4 熔融液中,其阴阳离子总数目为3NA | |
| D. | PH=1的盐酸溶液中,H+的数目为0.1NA |