题目内容
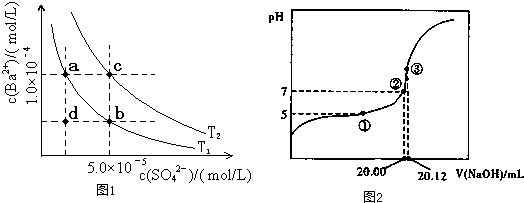
(1)不同温度下水的离子积的数据:25℃:1×10-14;t1:a; t2:1×10-12
试回答以下问题:
①若25<t1<t2,则a 1×10-14(填“>”、“<”或“=”),做此判断的理由是 .
②25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)= .
③在t2温度下测得某溶液pH=7,该溶液显 (填“酸”、“碱”或“中”)性.
(2)在一定温度下,有:a.醋酸 b.硫酸 c.盐酸三种酸:
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
(用a、b、c表示,下同)
②当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 .
反应所需时间的长短关系是 .
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 .
试回答以下问题:
①若25<t1<t2,则a
②25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,取该溶液1mL加水稀释至10mL,则稀释后溶液中c(Na+):c(OH-)=
③在t2温度下测得某溶液pH=7,该溶液显
(2)在一定温度下,有:a.醋酸 b.硫酸 c.盐酸三种酸:
①当三种酸物质的量浓度相同时,三种溶液中水的电离程度由大到小的顺序是
(用a、b、c表示,下同)
②当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为
反应所需时间的长短关系是
③将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:(1)①水是弱电解质,存在电离平衡,电离吸热;
②硫酸钠溶液是显中性的;
③t2温度下水的离子积常数是1×10-12,溶液为中性时溶液的pH=6;
(2)①酸溶液中氢离子浓度越大,水的电离程度越小,可以通过比较溶液中氢离子浓度判断种溶液中水的电离程度由大到小;
②氢离子浓度相同,醋酸是弱电解质,醋酸的浓度最大;刚开始反应时氢离子浓度相同,反应速率相等,之后醋酸能够电离出氢离子,溶液中氢离子浓度大于盐酸和硫酸溶液的,反应速率最快;
③醋酸是弱电解质,稀释过程中能够促进醋酸的电离,盐酸和硫酸属于强电解质,溶液中完全电离据此比较稀释后c(H+)由大到小.
②硫酸钠溶液是显中性的;
③t2温度下水的离子积常数是1×10-12,溶液为中性时溶液的pH=6;
(2)①酸溶液中氢离子浓度越大,水的电离程度越小,可以通过比较溶液中氢离子浓度判断种溶液中水的电离程度由大到小;
②氢离子浓度相同,醋酸是弱电解质,醋酸的浓度最大;刚开始反应时氢离子浓度相同,反应速率相等,之后醋酸能够电离出氢离子,溶液中氢离子浓度大于盐酸和硫酸溶液的,反应速率最快;
③醋酸是弱电解质,稀释过程中能够促进醋酸的电离,盐酸和硫酸属于强电解质,溶液中完全电离据此比较稀释后c(H+)由大到小.
解答:
解:(1)①水是弱电解质,存在电离平衡,电离吸热.所以温度升高,水的电离程度增大,离子积增大,
故答案为:>;温度升高,水的电离程度增大,离子积增大;
②25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中钠离子浓度是1×10-3 mol/L.如果稀释10倍,则钠离子浓度是1×10-4 mol/L.但硫酸钠溶液是显中性的,所以c(Na+):c(OH-)=10-4:10-7=1000:1,
故答案为:1000:1;
③t2温度下水的离子积常数是1×10-12,所以在该温度下,pH=6是显中性的.因此某溶液pH=7,该溶液显碱性,
故答案为:碱;
(2)①盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,所以当三种酸物质的量浓度相等时,溶液中c(H+)由大到小的顺序是b>c>a,氢离子浓度越大,水的电离程度越小,三种溶液中水的电离程度由大到小的顺序为:a>c>b,
故答案为:a>c>b;
②若三者c(H+)相同,则醋酸的浓度最大,所以物质的量浓度由大到小的顺序是c>a>b,开始时由于氢离子浓度相等,所以反应速率相等;之后由于醋酸能够电离出氢离子,醋酸溶液中氢离子浓度大于盐酸和硫酸的氢离子浓度,反应速率最大,反应时间最小,硫酸和盐酸反应的时间相等,反应所需时间的长短关系是:b=c>a,
故答案为:a=b=c;b=c>a;
③醋酸在稀释过程中,会促进电离,所以氢离子的物质的量增加,氢离子的浓度变化程度小,硫酸和盐酸溶液中氢离子物质的量不变且相等,所以c(H+)由大到小的顺序为:a>b=c,
故答案为:a>b=c.
故答案为:>;温度升高,水的电离程度增大,离子积增大;
②25℃时,某Na2SO4溶液中c(SO42-)=5×10-4 mol/L,则溶液中钠离子浓度是1×10-3 mol/L.如果稀释10倍,则钠离子浓度是1×10-4 mol/L.但硫酸钠溶液是显中性的,所以c(Na+):c(OH-)=10-4:10-7=1000:1,
故答案为:1000:1;
③t2温度下水的离子积常数是1×10-12,所以在该温度下,pH=6是显中性的.因此某溶液pH=7,该溶液显碱性,
故答案为:碱;
(2)①盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,所以当三种酸物质的量浓度相等时,溶液中c(H+)由大到小的顺序是b>c>a,氢离子浓度越大,水的电离程度越小,三种溶液中水的电离程度由大到小的顺序为:a>c>b,
故答案为:a>c>b;
②若三者c(H+)相同,则醋酸的浓度最大,所以物质的量浓度由大到小的顺序是c>a>b,开始时由于氢离子浓度相等,所以反应速率相等;之后由于醋酸能够电离出氢离子,醋酸溶液中氢离子浓度大于盐酸和硫酸的氢离子浓度,反应速率最大,反应时间最小,硫酸和盐酸反应的时间相等,反应所需时间的长短关系是:b=c>a,
故答案为:a=b=c;b=c>a;
③醋酸在稀释过程中,会促进电离,所以氢离子的物质的量增加,氢离子的浓度变化程度小,硫酸和盐酸溶液中氢离子物质的量不变且相等,所以c(H+)由大到小的顺序为:a>b=c,
故答案为:a>b=c.
点评:本题考查了水的电离、水的离子积常数和pH的有关计算、弱电解质的电离平衡以及离子浓度大小比较,题目难度中等,本题是基础性知识的考查,主要是巩固学生对教材基础知识的理解掌握程度,提高学生的解题能力.

练习册系列答案
相关题目
下列说法正确的是( )
| A、若反应X+Y=M+N是放热反应,该反应一定不用加热 |
| B、需要加热才能发生的反应一定是吸热反应 |
| C、原电池正极和负极的材料必须是两种金属 |
| D、铜锌原电池工作时,若有13g锌被溶解,外电路中就有0.4mol电子通过 |