题目内容
氨是没有颜色、有刺激性气味的气体,极易溶解于水且溶解得快,1体积水大约可溶解700体积氨气.在实验室里,常用氯化铵和氢氧化钙共热制取氨气.某同学用下列装置进行有关氨气制取及喷泉实验的探究,请回答.
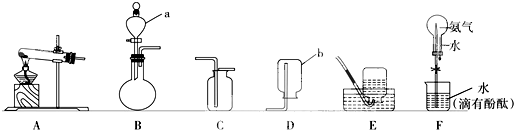
(1)写出图中所示仪器的名称:a ,b .
(2)实验室制取氨气的化学方程式为 .从图中选择相应的发生装置是 (填字母,下同),收集装置是 .
(3)某同学用收集有干燥纯净氨气的F装置进行实验观察到了红色喷泉.请描述他的关键操作是 .
(4)0℃101kPa 的条件下实验结束后,烧瓶中溶液的物质的量浓度为(溶质以NH3计算): .

(1)写出图中所示仪器的名称:a
(2)实验室制取氨气的化学方程式为
(3)某同学用收集有干燥纯净氨气的F装置进行实验观察到了红色喷泉.请描述他的关键操作是
(4)0℃101kPa 的条件下实验结束后,烧瓶中溶液的物质的量浓度为(溶质以NH3计算):
考点:氨的制取和性质
专题:实验设计题
分析:(1)根据仪器的特点确定仪器的名称;
(2)实验室用氯化铵和氢氧化钙加热制取氨气,反应物是固体,需要加热,据此确定制取的装置;氨气易溶于水,密度小于空气,据此确定收集的方法;
(3)氨气是极易溶于水的气体,氨气溶于水后,烧瓶内压强减少,产生压强差,导致溶液进入烧瓶;
(4)根据C=
计算其物质的量浓度.
(2)实验室用氯化铵和氢氧化钙加热制取氨气,反应物是固体,需要加热,据此确定制取的装置;氨气易溶于水,密度小于空气,据此确定收集的方法;
(3)氨气是极易溶于水的气体,氨气溶于水后,烧瓶内压强减少,产生压强差,导致溶液进入烧瓶;
(4)根据C=
| n |
| V |
解答:
解:)根据仪器的特点确定仪器的名称a是分液漏斗;b是集气瓶,故答案为:分液漏斗;集气瓶;
(2)在加热条件下,氯化铵和氢氧化钙反应生成氯化钙、氨气和水,2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,反应物是固体,需要加热来制取的气体可以选择装置A,氨气易溶于水,密度小于空气,可以采用向上排空气法收集,即选择D装置,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;A;D;
(3)NH3极易溶解于水,1体积水溶解700体积氨气,打开止水夹挤出胶头滴管中的水,然后打开止水夹K,由于氨气迅速溶解在挤出胶头滴管中的水,导致烧瓶内气体压强迅速减小,导致溶液进入烧瓶产生喷泉现象,故答案为:轻轻挤压滴管,使少量水加入烧瓶,然后打开止水夹;
(4)据题意知,实验溶解于水的氨气占满烧瓶,设烧瓶的体积是V,氨水溶液的浓度c(NH3)=
mol/L=
mol/L,故答案为:
mol/L.
(2)在加热条件下,氯化铵和氢氧化钙反应生成氯化钙、氨气和水,2NH4Cl+Ca(OH)2
| ||
| ||
(3)NH3极易溶解于水,1体积水溶解700体积氨气,打开止水夹挤出胶头滴管中的水,然后打开止水夹K,由于氨气迅速溶解在挤出胶头滴管中的水,导致烧瓶内气体压强迅速减小,导致溶液进入烧瓶产生喷泉现象,故答案为:轻轻挤压滴管,使少量水加入烧瓶,然后打开止水夹;
(4)据题意知,实验溶解于水的氨气占满烧瓶,设烧瓶的体积是V,氨水溶液的浓度c(NH3)=
| ||
| V |
| 1 |
| 22.4 |
| 1 |
| 22.4 |
点评:本题主要考查了氨的实验室制备原理以,掌握氨的实验室制法以及物质的性质是解答的关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温常压下,下列化合物以液态形式存在的是( )
| A、甲醛 | B、二氯甲烷 |
| C、丙烯 | D、丁烷 |
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的最高价氧化物的对应水化物是一种强酸;Z的非金属性在同周期主族元素中最强.
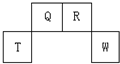 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题: