题目内容
10.标准状况下,若2.8LO2含有n个O2分子,则阿伏加德罗常数为( )| A. | n/8 | B. | n/16 | C. | 8n | D. | 16n |
分析 根据n=$\frac{V}{{V}_{m}}$计算标准状况下2.8L氧气的物质的量,根据N=nNA计算阿伏伽德罗常数.
解答 解:标准状况下,2.8L氧气的物质的量为$\frac{2.8L}{22.4L/mol}$=$\frac{1}{8}$mol,
所以$\frac{1}{8}$mol×NA=n,解之得:NA=8nmol-1,
故选:C.
点评 本题考查阿伏伽德罗常数的计算,难度不大,注意公式运用,明确体积、物质的量、微粒数目的关系是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列关于有机化合物的说法正确的是( )
| A. | 2-甲基丁烷也称为异丁烷 | |
| B. | 苯乙烯(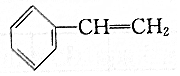 )分子中所有原子都可能共平面 )分子中所有原子都可能共平面 | |
| C. | 一氯甲烷、二氯甲烷互为同系物 | |
| D. | 油脂和蛋白质都属于高分子化合物 |
18.实验室有两瓶失去标签的溶液,其中一瓶是Na2CO3溶液,另一瓶是NaOH溶液,浓度均未知.鉴别时,下列选用的试纸或试剂不正确的是( )
| A. | 酚酞溶液 | B. | HCl溶液 | C. | BaCl2溶液 | D. | Ba(OH)2溶液 |
15.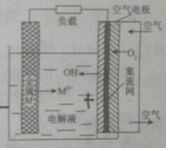 金属燃料电池是一类特殊的燃料电池.具有成本低、无毒、无污染、比功率高、比能量高等优点,电池的基本结构如图,锌、铁、镁、铝等金属都可以用在金属燃料电池中.下列说法不正确的是( )
金属燃料电池是一类特殊的燃料电池.具有成本低、无毒、无污染、比功率高、比能量高等优点,电池的基本结构如图,锌、铁、镁、铝等金属都可以用在金属燃料电池中.下列说法不正确的是( )
 金属燃料电池是一类特殊的燃料电池.具有成本低、无毒、无污染、比功率高、比能量高等优点,电池的基本结构如图,锌、铁、镁、铝等金属都可以用在金属燃料电池中.下列说法不正确的是( )
金属燃料电池是一类特殊的燃料电池.具有成本低、无毒、无污染、比功率高、比能量高等优点,电池的基本结构如图,锌、铁、镁、铝等金属都可以用在金属燃料电池中.下列说法不正确的是( )| A. | 电池工作时.金属M电极皱氧化.发生氧化反应 | |
| B. | 电池工作时.空气电极反应式为O2+4e-+2H2O=4OH | |
| C. | 电池工作时.OH-向负极移动,负极附近溶液的pH增大 | |
| D. | 若M为锌,电池反应方程式为2Zn+2H2O+O2=2Zn(OH)2 |
5.亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2═LiNH2+LiH;则下列有关说法正确的是( )
| A. | Li2NH中N的化合价是-1 | B. | 此法储氢和钢瓶储氢的原理相同 | ||
| C. | H+与H -的离子半径均比Li+大 | D. | 该反应中H2既是氧化剂又是还原剂 |
2.X、Y、Z三种主族元素,已知X+和Y-具有相同的电子层结构,Z元素原子核电荷数比Y元素原子核电荷数少9,Y-在一定条件下可被氧化成YZ3-,则下列说法正确的是( )
| A. | X、Y、Z均属于短周期元素 | |
| B. | 离子半径X+>Y- | |
| C. | X、Y、Z三种元素只能形成化合物XYZ3 | |
| D. | Y的气态氢化物的热稳定性可能较强 |
20.下列实验方法能达到实验目的是( )
| A. | 用湿润的红色石蕊试纸检验氨气 | |
| B. | 用长颈漏斗分离碘的四氯化碳溶液和水溶液 | |
| C. | 用焰色反应鉴别NaCl和Na2SO4两种无色晶体 | |
| D. | 用KSCN溶液鉴别FeCl3溶液和Fe(NO3)3溶液 |
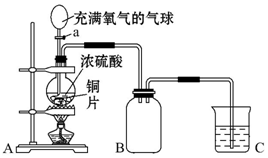
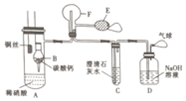 为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个被固定的干燥管,内装块状碳酸钙固体;F为一个空的蒸馏烧瓶;E是用于鼓入空气的双连打气球.
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个被固定的干燥管,内装块状碳酸钙固体;F为一个空的蒸馏烧瓶;E是用于鼓入空气的双连打气球.