题目内容
下列属于含共价键的分子晶体的是( )
| A、干冰 | B、二氧化硅 |
| C、固态氩 | D、NaOH晶体 |
考点:化学键,分子晶体
专题:化学键与晶体结构
分析:分子晶体是分子间通过分子间作用力(包括范德华力和氢键)构成的晶体.常见的分子晶体有:所有非金属氢化物、部分非金属单质(金刚石、晶体硅等除外)、部分非金属氧化物(二氧化硅等除外)、几乎所有的酸、绝大多数的有机物晶体、所有常温下呈气态的物质、常温下呈液态的物质(除汞外)、易挥发的固态物质等.
解答:
解:A、干冰是通过分子间作用力结合在一起的分子晶体,氧原子和碳原子形成共价键,故A正确;
B、二氧化硅是由Si和O以共价键结合在一起的原子晶体,故B错误;
C、固态氩是直接由原子构成的分子晶体,不含共价键,故C错误;
D、NaOH晶体是由钠离子和氢氧根离子组成的离子晶体,故D错误;
故选A.
B、二氧化硅是由Si和O以共价键结合在一起的原子晶体,故B错误;
C、固态氩是直接由原子构成的分子晶体,不含共价键,故C错误;
D、NaOH晶体是由钠离子和氢氧根离子组成的离子晶体,故D错误;
故选A.
点评:本题考查常见物质晶体类型判断等,难度不大,掌握常见物质晶体类型及常见分子晶体.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
下列基态原子的电子排布图中,正确的是( )
A、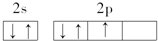 |
B、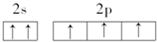 |
C、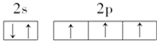 |
D、 |
下列说法正确的是( )
A、萘(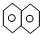 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 )是最简单的稠环芳香烃,萘与足量氢气充分加成的产物一氯代物有2种 |
B、酚酞的结构如图所示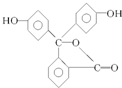 ,其结构中含有羟基(-OH),故酚酞属于醇 ,其结构中含有羟基(-OH),故酚酞属于醇 |
| C、溴水能将甲苯、己烯、CCl4、乙醇四种溶液鉴别开来 |
D、 的名称为2-甲基-4-戊醇 的名称为2-甲基-4-戊醇 |
金属钠分别与下列溶液反应时,既有气体又有沉淀产生的是( )
| A、Na2CO3 |
| B、NH4Cl |
| C、BaCl2 |
| D、FeCl3 |
欲提取碘水中的碘,不能选用的萃取剂是( )
| A、苯 | B、四氯化碳 |
| C、蒸馏汽油 | D、酒精 |
根据元素周期表和元素周期律的下列推断,其中错误的是( )
| A、铍(Be)的原子失电子能力比镁弱 |
| B、砹(At)的氢化物不稳定 |
| C、砷酸(H3AsO4)比磷酸的酸性强 |
| D、硫酸锶(SrSO4)是难溶于水的白色固体 |
下列除杂质的方法中正确的是( )
| A、乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液 |
| B、乙烷中混有乙烯,通入H2,在一定条件下反应使乙烯完全转化成乙烷 |
| C、苯甲醛中混有苯甲酸,加入生石灰后,再加热蒸馏 |
| D、溴苯中含有单质溴加入KI溶液后用分液漏斗分液 |
下列叙述正确的是( )
| A、CO2分子内存在着非极性共价键 |
| B、SO2与H2O反应的产物是离子化合物 |
| C、CO2分子内存在着极性共价键 |
| D、盐酸溶液中含H+和Cl-故HCl为离子化合物 |
下列各组元素中,第一电离能依次减小的是( )
| A、H Li Na K |
| B、Na Mg Al Si |
| C、I Br Cl F |
| D、F O N C |