题目内容
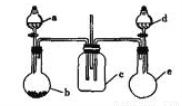
(本小题14分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
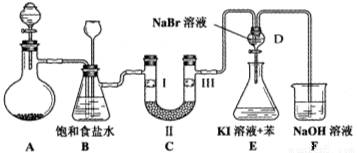
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:________________________。
(2)装置B中饱和食盐水的作用是________________________________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__________。
| A | B | C | D |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是 。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_______________________________。
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因_____________________________________。
17.(本小题14分,每空2分)(1)Ca(ClO)2+4HCl(浓)==CaCl2+2Cl2↑+2H2O
(2)除去Cl2中HCl ;B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降;(3)D
(4)比较氯、溴、碘的非金属性强弱 E中溶液分为两层,上层液体为紫红色
(5)4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O。
【解析】
试题分析:(1)漂粉精固体的有效成分是Ca(ClO)2,它和浓盐酸反应的化学反应方程式为Ca(ClO)2+4HCl(浓)==CaCl2+2Cl2↑+2H2O;(2)由于浓盐酸有挥发性,所以在制取的Cl2中含有HCl杂质,装置B中饱和食盐水的作用是除去Cl2中HCl;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象B中长颈漏斗内液面上升,形成一段水柱,锥形瓶内液面下降;(3)装置C的实验目的是验证氯气是否具有漂白性,所以Ⅰ中湿润的有色布条,看到褪色;由于是在U型管,所以应该是固体干燥剂,而浓硫酸是液体,不能使用,所以Ⅱ中放无水氯化钙来吸收水,Ⅲ中放干燥的有色布条不褪色,证明有漂白作用的是HClO,而不是Cl2。选项是D。(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。打开活塞,将装置D中少量溶液加入装置E中,振荡。由于Cl2会与NaBr、KI发生氧化还原反应产生Br2、I2, I2容易溶解在苯中,苯与水互不相溶,I2溶解在苯中得到的溶液是紫色,因此会观察到的现象是E中溶液分为两层,上层液体为紫红色;(5)氯气能够与NaOH发生反应产生无毒的物质,但是某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,但是老师认为不妥,原因是氯气与水发生反应产生的HClO把NaHSO3氧化为SO42-。还会发生产生的盐酸会与NaHSO3发生反应产生SO2,用总反应的离子方程式解释是4HSO3-+Cl2=SO42-+2Cl-+3SO2+2H2O。
考点:考查氯气的制取、性质验证、实验现象、操作方法及两种方程式的书写的知识。

下列选项中的原因或结论与现象不对应的是
选项 | 现象 | 原因或结论 |
A | 在 H2O2中加入MnO2,能加速H2O2的分解速率 | MnO2降低了反应所需的活化能 |
B | 向5mL 0.005mol·L-1FeCl3溶液中加入5mL 0.015mol·L-1KSCN溶液,溶液呈红色,再滴加几滴1mol·L-1KSCN溶液,溶液颜色加深 | 增大反应物浓度,平衡向正反应方向移动 |
C | 将盛有NO2气体的密闭容器浸泡在热水中,容器内气体颜色变深 | 该反应△H<0,平衡向生成NO2方向移动 |
D | 在密闭容器中有反应:A+xB(g) | A非气体、x=1 |
 2C(g)。达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的两倍,测得c(A)为0.4mol/L-1
2C(g)。达到平衡时测得c(A)为0.5mol/L,将容器容积扩大到原来的两倍,测得c(A)为0.4mol/L-1 )原子核内有1个质子
)原子核内有1个质子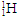 与
与