题目内容
下列叙述中,正确的是( )
| A、氧化还原反应的本质是元素化合价发生了变化 |
| B、所含元素化合价升高的反应物被氧化 |
| C、得到电子的物质被氧化 |
| D、氧化还原反应中,氧化剂和还原剂一定是两种物质 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.本质为电子的转移;
B.元素的化合价升高,则失去电子;
C.得到电子的物质为氧化剂;
D.氧化还原反应中,同种元素可能既失去电子也得到电子.
B.元素的化合价升高,则失去电子;
C.得到电子的物质为氧化剂;
D.氧化还原反应中,同种元素可能既失去电子也得到电子.
解答:
解:A.氧化还原反应的特征是元素化合价发生了变化,其本质为电子的转移,故A错误;
B.元素的化合价升高,则失去电子,被氧化,发生氧化反应,故B正确;
C.得到电子的物质为氧化剂,在反应中被还原,故C错误;
D.氧化还原反应中,同种元素可能既失去电子也得到电子,如氯气与水的反应,氧化剂、还原剂可为同种物质,故D错误;
故选B.
B.元素的化合价升高,则失去电子,被氧化,发生氧化反应,故B正确;
C.得到电子的物质为氧化剂,在反应中被还原,故C错误;
D.氧化还原反应中,同种元素可能既失去电子也得到电子,如氯气与水的反应,氧化剂、还原剂可为同种物质,故D错误;
故选B.
点评:本题考查氧化还原反应,为高频考点,把握氧化还原反应基本概念为解答的关键,注意氧化还原反应本质、特征、氧化与还原反应及常见的实例,题目难度不大.

练习册系列答案
相关题目
下列元素中,化学性质和物理性质最像Q元素的是( )
| A、硼(1s22s22p1) |
| B、铍(1s22s2) |
| C、锂(1s22s1) |
| D、氦(1s2) |
用一种试剂鉴别四氯化碳、苯酚、己烯、碘化钾溶液、苯五种液体,可选用( )
| A、盐酸 |
| B、FeCl3溶液 |
| C、溴水 |
| D、四氯化碳 |
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通入乙烷和氧气,其电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O 7H2O+
O2+14e-=14OH-,有关此电池的推断正确的是( )
| 7 |
| 2 |
| A、通氧气的电极为负极 |
| B、参加反应的氧气与C2H6的物质的量之比为7:2 |
| C、放电一段时间后,KOH的物质的量浓度不变 |
| D、电解质溶液中,CO32-向正极移动 |
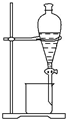
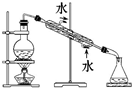
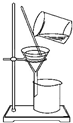
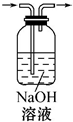
完成下列实验所需选择的装置或仪器都正确的是( )
| A | B | C | D | |
| 实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的氯化钾晶体 | 分离CCl4中的Br2 | 除去CO2气体中的HCl气体 |
| 装置 或仪器 |
 |
 |
 |
 |
| A、A | B、B | C、C | D、D |
在一个化学实验室内桌上放着四瓶化学试剂,瓶壁标签上分别写着葡萄糖、淀粉、食盐、味精.为了进一步确认它们的实物和名称是否相符而进行化学实验,下列做法中不可取的是( )
| A、观察、比较它们的外观状态 |
| B、各取少量分别放在手里试试重量 |
| C、各取少量分别放入口里品尝一下味道 |
| D、使用化学方法进行鉴别 |
下列说法中,正确的是( )
| A、强电解质的水溶液一定比弱电解质溶液的导电能力强 |
| B、强电解质都是离子化合物,弱电解质都是共价化合物 |
| C、强电解质的水溶液中不存在溶质分子 |
| D、不溶性盐都是弱电解质,可溶性酸和具有极性键的化合物都是强电解质 |
已知微粒MnO4-、Cl2、Fe3+、Cu2+、H+在溶液中的氧化性强弱顺序为MnO4->Cl2>Fe3+>Cu2+>H+,则下列反应能发生的是( )
①2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O
②Cl2+2Fe2+═2Fe3++2Cl-
③2Fe3++Cu═2Fe2++Cu2+
④Cu+2H+═Cu2++H2↑
①2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O
②Cl2+2Fe2+═2Fe3++2Cl-
③2Fe3++Cu═2Fe2++Cu2+
④Cu+2H+═Cu2++H2↑
| A、①② | B、①②④ |
| C、①②③④ | D、①②③ |
20gA物质和14gB物质恰好完全反应,生成8.8gC物质、6.0gD物质和0.2molE物质,则E物质的摩尔质量为( )
| A、100g/mol |
| B、108g/mol |
| C、96g/mol |
| D、55g/mol |