题目内容
短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,且原子最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子;A与C,B与D均为同主族元素.下列叙述正确的是( )
| A、B元素组成的一种单质具有漂白性,能使KMnO4溶液紫色褪去 |
| B、B、D两种元素形成的一种化合物也具有一定的漂白性,能使紫色石蕊紫色褪去 |
| C、C元素分别与A元素和B元素形成的化合物都是离子晶体,一定均与水反应生成强碱和无色气体 |
| D、A2B的热稳定性强于A2D、沸点也高于A2D,但解释的理由不相同 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素A、B、C、D的原子序数依次增大,A与C,B与D均为同主族元素,则B与D分别位于第二、第三周期.
B位于第二周期,次外层电子数为2,A、C原子的最外层电子数之和等于B原子的次外层电子,则A、C的最外层电子数为1,则A、C处于第ⅠA族.
A、B、C、D的原子最外层电子数之和为14,则B、D的原子最外层电子数为
=6,所以B为氧元素,D为硫元素.
A、B、C、D的原子序数之和为36,所以A、C的原子序数之和为36-8-16=12,所以A为氢元素,C为钠元素.
B位于第二周期,次外层电子数为2,A、C原子的最外层电子数之和等于B原子的次外层电子,则A、C的最外层电子数为1,则A、C处于第ⅠA族.
A、B、C、D的原子最外层电子数之和为14,则B、D的原子最外层电子数为
| 14-1×2 |
| 2 |
A、B、C、D的原子序数之和为36,所以A、C的原子序数之和为36-8-16=12,所以A为氢元素,C为钠元素.
解答:
解:A.B为氧元素,形成的单质有氧气和臭氧,二者均不能使KMnO4溶液紫色褪去,故A错误;
B.B为氧元素,D为硫元素,二者形成的二氧化硫也具有一定的漂白性,能使紫色石蕊变蓝,但不能褪色,故B错误;
C.A为氢元素,B为氧元素,C为钠元素,C元素分别与A元素和B元素形成的化合物中有氧化钠,氧化钠和水反应只生成强碱氢氧化钠,没有无色气体生成,故C错误;
D.A为氢元素,B为氧元素,D为硫元素,H2O比H2S热稳定性强是因为O-H键能比S-H键能大,H2O比H2S沸点高是由于H2O间形成氢键,故D正确.
故选:D.
B.B为氧元素,D为硫元素,二者形成的二氧化硫也具有一定的漂白性,能使紫色石蕊变蓝,但不能褪色,故B错误;
C.A为氢元素,B为氧元素,C为钠元素,C元素分别与A元素和B元素形成的化合物中有氧化钠,氧化钠和水反应只生成强碱氢氧化钠,没有无色气体生成,故C错误;
D.A为氢元素,B为氧元素,D为硫元素,H2O比H2S热稳定性强是因为O-H键能比S-H键能大,H2O比H2S沸点高是由于H2O间形成氢键,故D正确.
故选:D.
点评:本题考查位置结构性质关系、元素化合物知识,难度中等,利用提供数据及位置关系推断元素是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温下,下列分子或离子在指定条件下一定能大量共存的是( )
| A、饱和Na2CO3溶液中:NH4+、C6H5OH、NO3-、NH3?H2O |
| B、潮湿的Cl2中:CO2、N2、SO2、C2H4 |
| C、通入NO2气体的溶液中:K+、Fe2+、I-、SO42- |
| D、无水C2H5OH中:Na+、K+、OH-、C2H5Br |
在pH=1的溶液中,可以大量共存的离子组是( )
| A、Na+、K+、S2-、Cl- |
| B、Al3+、HCO3-、SO42-、Cl- |
| C、K+、Na+、SiO32-、NO3- |
| D、K+、Cl-、SO42-、NO3- |
 着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲.红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示.下列说法正确的是( )
着色剂为使食品着色的物质,可增加对食品的嗜好及刺激食欲.红斑素、红曲素是常用于糖果、雪糕等食品的着色剂的主要成分,结构如图所示.下列说法正确的是( )| A、红斑素和红曲素互为同分异构体 |
| B、红斑素中含有醚键、羰基、酯键这三种含氧官能团 |
| C、一定条件下红斑素和红曲素都能发生加聚和缩聚反应 |
| D、1 mol红曲素最多能与6 mol H2发生加成反应 |
 短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是( )
短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是( )| A、原子半径:丙<丁<戊 |
| B、金属性:甲>丙 |
| C、氢氧化物碱性:丙>丁>戊 |
| D、最外层电子数:甲>乙 |
若NA代表阿伏加德罗常数,则下列叙述正确的是( )
| A、16g氧气和臭氧的混合物中原子的数目0.5NA |
| B、1mol Cl2与足量的铁完全反应,转移的电子数为2NA |
| C、1 L 0.5mol?L-1 AlCl3溶液中含有的Al3+数目为0.5NA |
| D、在标准状况下,22.4L HCl与22.4L H2O2所含有的电子数均为18 NA |
下列说法正确的是( )
| A、一定温度下,将盐酸滴加入醋酸钠溶液中至呈中性.此时溶液中:c(Na+)>c(Cl-)=c(CH3COOH) |
| B、常温下,将0.1 mol?L-1氨水稀释10倍后,其pH大于12 |
| C、常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO4)=4.9×10-5,则反应CaSO4(s)+CO32- (aq)═CaCO3(s)+SO42-(aq) 平衡常数K约为1.75×10-4 |
| D、溶有等物质的量的NaClO、NaHCO3的混合溶液中:c(HClO)+c(ClO-)=c(CO32-)+c(HCO3-)+c(H2CO3) |
 黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为:
黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为: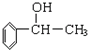 (1)苏合香醇可以用作食用香精,其结构简式如图所示.
(1)苏合香醇可以用作食用香精,其结构简式如图所示.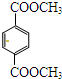 的同分异构体有多种,满足下列条件的共有
的同分异构体有多种,满足下列条件的共有