题目内容
3.下列有关电解质溶液的说法正确的是( )| A. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(C{l}^{-})}$<1 | |
| B. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$变大 | |
| C. | 将CH3COONa溶液加入水稀释后,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| D. | 向0.1 mol•L-1 CH3COOH溶液从20℃升温至30℃,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 |
分析 A.溶液中存在电荷守恒分析;
B.饱和溶液中存在溶度积常数只随温度变化不随浓度变化;
C.醋酸钠溶液中醋酸根离子水解,水解平衡常数不随浓度变化;
D.醋酸为弱电解质存在电离平衡,升温平衡正向进行;
解答 解:A.向盐酸中加入氨水至中性,c(H+)=c(OH-),溶液中存在电荷守恒,c(H+)+c(NH4+)=c(Cl-)+c(OH-),则c(NH4+)=c(Cl-),$\frac{c(N{{H}_{4}}^{+})}{c(C{l}^{-})}$=1,故A错误;
B.向AgCl、AgBr的饱和溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$=$\frac{c(C{l}^{-})}{c(B{r}^{-})}$×$\frac{c(A{g}^{+})}{c(A{g}^{+})}$=$\frac{Ksp(AgCl)}{Ksp(AgBr)}$,加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$不变,故B错误;
C.将CH3COONa溶液加入水稀释后促进水解,CH3COO-+H2O?CH3COOH+OH-,K=$\frac{c(O{H}^{-})c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$,温度不变,K不变,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)c(O{H}^{-})}$不变,故C正确;
D.向0.1 mol•L-1 CH3COOH溶液从20℃升温至30℃,促进醋酸电离,氢离子物质的量增大,醋酸物质的量减小,则$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$增大,故D错误;
故选C.
点评 本题考查了弱电解质电离平衡、沉淀溶解平衡、盐类水解平衡的影响因素,平衡常数只随温度变化不随浓度变化,掌握基础是解题关键,题目难度中等.

| A. | 平衡常数 | B. | HI的平衡浓度 | ||
| C. | 达到平衡的时间 | D. | 平衡时H2的体积分数 |
| A. | N、M均不能发生银镜反应 | B. | M中可能没有甲基 | ||
| C. | N可发生消去反应 | D. | N分子中含有甲基 |
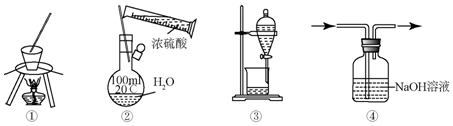
| A. | ①用于实验室从食盐水中提取氯化钠 | |
| B. | ②配制一定物质的量浓度的硫酸溶液 | |
| C. | ③用于苯萃取碘水中的碘后放出碘的苯溶液 | |
| D. | ④用于除去CO中混有的CO2 |
| A. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| B. | 加入水,平衡向逆反应方向移动 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,溶液中C(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
| A. | 提高反应温度 | B. | 移出部分CO2 | ||
| C. | 加入合适的催化剂 | D. | 减小容器的容积 |
| A. | 甲醇的结构式:CH4O | |
| B. | 钠离子的结构示意图: | |
| C. | 质子数为16、中子数为17的硫原子:${\;}_{16}^{17}$S | |
| D. | 硫化氢分子的电子式: |
 →
→
下列说法正确的是( )
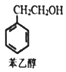
| A. | 苯乙醇分子中含有1个手性碳原子 | |
| B. | 与苯乙醇互为同分异构体的芳香醇有4种 | |
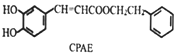
| C. | 苯乙醉及CPAE都能发生取代、加成和消去反应 | |
| D. | 1 mol CPAE最多可与含3 molNaOH的溶液发生反应 |