题目内容
将1molNa和1molAl的混合物投入足量水中,产生气体在标准状况下的体积为( )
分析:首先发生反应:2Na+2H2O=2NaOH+H2↑,根据钠计算生成氢气、氢氧化钠的物质的量,然后发生2Al+2NaOH+2H2O═2NaAlO2+3H2↑,进行过量计算,根据不足量的物质的量计算生成氢气的物质的量,两部分氢气之和为总的氢气的物质的量,再个V=nVm计算体积.
解答:解:首先1molNa与水反应,则:
2Na+2H2O=2NaOH+H2↑
1mol 1mol 0.5mol
然后发生反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑,由方程式可知1molAl消耗1molNaOH,故Al与NaOH恰好完全反应,生成氢气为1mol×
=1.5mol,
故生成氢气的总体积为(0.5mol+1.5mol)×22.4L/mol=44.8L,
故选D.
2Na+2H2O=2NaOH+H2↑
1mol 1mol 0.5mol
然后发生反应2Al+2NaOH+2H2O═2NaAlO2+3H2↑,由方程式可知1molAl消耗1molNaOH,故Al与NaOH恰好完全反应,生成氢气为1mol×
| 3 |
| 2 |
故生成氢气的总体积为(0.5mol+1.5mol)×22.4L/mol=44.8L,
故选D.
点评:本题考查混合物的有关计算,难度不大,清楚发生的反应是关键,注意铝与氢氧化钠反应的过量计算.

练习册系列答案
相关题目
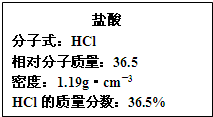 试回答下列问题:
试回答下列问题: