题目内容
将H2S气体通入FeCl2、ZnSO4溶液中,不能生成FeS、ZnS沉淀的原因是 ,而通入CuSO4溶液中,能产生CuS沉淀的原因是 .
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:在FeSO4、ZnSO4溶液中通入适量H2S,硫酸亚铁、ZnSO4和硫化氢不反应,硫酸铜和硫化氢反应生成硫化铜沉淀,硫化铜沉淀难溶于水和酸.
解答:
解:在FeSO4、ZnSO4溶液中通入适量H2S,硫酸亚铁、ZnSO4和硫化氢不反应,因为硫化亚铁和硫酸锌都可以溶解于生成的强酸硫酸中,但是硫酸铜和硫化氢反应生成硫化铜沉淀,难溶于水和硫酸中.
故答案为:FeS、ZnS沉淀能溶于硫酸中;CuS沉淀不溶于硫酸.
故答案为:FeS、ZnS沉淀能溶于硫酸中;CuS沉淀不溶于硫酸.
点评:本题考查学生复分解反应的原理以及物质的性质知识,注意知识的归纳和梳理是关键,难度中等.

练习册系列答案
相关题目
下列物质在水溶液中的电离方程式正确的是( )
| A、Na2CO3=Na22++CO32- |
| B、NaHSO4=Na++H++SO42- |
| C、CH3COOH=H++CH3COO- |
| D、H2CO3=2H++CO32- |
下列溶液中各微粒的浓度关系正确的是( )
| A、0.1mol?L-1HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B、0.1mol?L-1NaHCO3溶液中:c(Na+)+c(H+)十c(H2CO3)=c(HCO3-)+2c(CO32-) |
| C、等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| D、等物质的量浓度的硫酸与醋酸钠溶液等体积混合:2c(SO42-)+c(OH-)=c(H+)+c(CH3COOH) |
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量).下列判断正确的是( )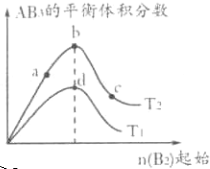

| A、若T2>T1,达到平衡时b、d点的反应速率为vd>vb |
| B、若T2>T1,则正反应一定是放热反应 |
| C、达到平衡时A2的转化率大小为b>a>c |
| D、在T2和n(A2)不变时达到平衡,AB3的物质的量大小为c>b>a |
某同学按图所示的装置进行电解实验.下列说法正确的是( )
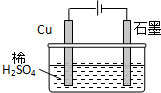

| A、电解过程中,铜电极上有H2产生 | ||||
| B、电解一定时间后,石墨电极上有H2析出 | ||||
| C、整个电解过程中,H+的浓度不断增大 | ||||
D、电解初期,主反应方程式为:Cu+H2SO4
|
实验室需配制一种强酸溶液500mL,且要求c (H+)=2mol/L,下列配制方法可行的是( )
| A、取100mL5mol/LH2SO4,加入400mL水 |
| B、取200mL5mol/LHCl,加水稀释至500mL |
| C、取100 mL5mol/LH2SO4,加水500mL |
| D、取100 mL5mol/LHNO3,加水稀释至500mL |
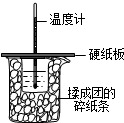 50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol?L-1盐酸与50mL0.55mol?L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: 和
和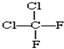 ; ⑨
; ⑨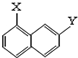 和
和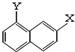 .
.