题目内容
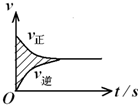 在容积固定的2L 密闭容器中进行着一个可逆反应X(g)+2Y(g)?2Z(g),用Y的物质的量浓度改变表示的反应速率v正、v逆与时间的关系如图所示.已知v的单位为mol?(L?s)-1,则图中阴影部分的面积表示( )
在容积固定的2L 密闭容器中进行着一个可逆反应X(g)+2Y(g)?2Z(g),用Y的物质的量浓度改变表示的反应速率v正、v逆与时间的关系如图所示.已知v的单位为mol?(L?s)-1,则图中阴影部分的面积表示( )| A、X的物质的量浓度的减少 |
| B、Y的物质的量浓度的减少 |
| C、Z的物质的量的增加 |
| D、Y的物质的量的减少 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:观察图象,纵坐标为Y的反应速率,横坐标为时间,由微分法可知,二者之积为浓度,故V(正)×t(平衡)表示Y向正反应方向进行时减少的浓度,V(逆)×t(平衡)表示B向逆反应方向进行时增大的浓度,故阴影部分的面积表示Y向正反应方向进行时“净”减少的浓度,再利用浓度变化量之比等于化学计量数之比判断X的浓度变化,据此解答.
解答:
解:V(正)×t(平衡)表示Y向正反应方向进行时减少的浓度,V(逆)×t(平衡)表示Y向逆反应方向进行时增大的浓度,故阴影部分的面积表示Y向正反应方向进行时“净”减少的浓度,即阴影为平衡时Y的浓度减少量△c(Y),
A、浓度变化量之比等于化学计量数之比,故△c(X)=
△c(Y),为阴影面积的一半,故A错误;
B、由上述分析可知,阴影为平衡时Y的浓度减少量△c(Y),故B正确;
C、由上述分析可知,阴影为平衡时Y的浓度减少量△c(Y),故C错误;
D、阴影为平衡时Y的浓度减少量△c(Y),容器的体积为2L,阴影部分的面积不能表示Y的物质的量的减少量,故D错误;
故选B.
A、浓度变化量之比等于化学计量数之比,故△c(X)=
| 1 |
| 2 |
B、由上述分析可知,阴影为平衡时Y的浓度减少量△c(Y),故B正确;
C、由上述分析可知,阴影为平衡时Y的浓度减少量△c(Y),故C错误;
D、阴影为平衡时Y的浓度减少量△c(Y),容器的体积为2L,阴影部分的面积不能表示Y的物质的量的减少量,故D错误;
故选B.
点评:本试题为化学平衡知识的考查,难度较大,可以借助数学微分方法理解v-t时间图象中所围区域面积的含义.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
不属于天然高分子化合物的是( )
| A、淀粉 | B、纤维素 |
| C、葡萄糖 | D、蛋白质 |
洗涤盛有植物油的试管,宜选用的试剂是( )
| A、稀硫酸 | B、热水 |
| C、热碱液 | D、稀硝酸 |
在1.5L的密闭容器中通入2molN2和3molH2的混合气体,在一定条件下发生反应.达到平衡时,容器内压强为反应开始时的0.8,则该反应的化学平衡常数为( )
| A、0.20mol-2?L2 |
| B、0.20 |
| C、0.44mol-2?L2 |
| D、0.44 |
下列物质未纳入我国空气质量报告的是( )
| A、二氧化硫 | B、氮的氧化物 |
| C、甲醛 | D、悬浮颗粒物 |
已知下列反应:Co2O3+6HCl(浓)═2CoCl2+Cl2↑+3H2O(Ⅰ);5Cl2+I2+6H2O═10HCl+2HIO3(Ⅱ).
下列说法正确的是( )
下列说法正确的是( )
| A、还原性:CoCl2>HCl>I2 |
| B、氧化性:Co2O3>Cl2>HIO3 |
| C、反应Ⅰ中HCl是氧化剂 |
| D、反应Ⅱ中Cl2发生氧化反应 |
如图是电解精炼铜装置,其中c、d为铜电极.则下列有关的判断不正确的是( )


| A、c为粗铜板、d为纯铜板 |
| B、电解过程中,SO42-浓度几乎不变 |
| C、电解过程中,阳极质量的减少与阴极质量的增加相等 |
| D、电解过程中,c电极板附近沉积不溶物,d电极板质量增加 |
在两个容积相同的容器中,一个盛有NH3,另一个盛有N2、H2的混合气体,在同温同压下,两容器内的气体一定具有相同的( )
| A、原子数 | B、分子数 |
| C、质量 | D、密度 |