��Ŀ����
15�������۵�660�棩��һ��Ӧ�ù㷺�Ľ�������ҵ����Al2O3���۵�2045�棩�ͱ���ʯ��NaAlF6�������������ƣ�������ں����Ƶã��ش����м��⣺��1��ұ��ҵ�ϳ��ý���������ԭ��ұ�����������̣�����V2O3�ڸ����·�Ӧ�Ļ�ѧ����ʽΪV2O3+2Al$\frac{\underline{\;����\;}}{\;}$2V+Al2O3��
��2������ĥ������Ƭ�ھƾ��ƻ����ϼ��ȣ��ɹ۲쵽���ۻ��������䣬ԭ��������������Ӧ�������������۵�ߣ����ǻ��ý���������ĥ������ƬͶ���ˮ�в��۲쵽�����ݲ�����������Ƭ�ñ���Hg��NO3��2��Һ���������ӣ�ȡ����Ѹ��ϴ�������Ƶ��׳ơ������롰�������Ͻ�������¶���ڿ����У������������������ɵİ�ë��Al2O3�����������Ƶ����������ˮ�У���Ѹ�ٷ�Ӧ�������ݣ��÷�Ӧ�Ļ�ѧ����ʽ��2Al+6H2O=2Al��OH��3+3H2����������Ļ�ѧ���ʱ�á����á���ԭ������DZ��治�����γ���������Ĥ��
��3����0.1mol•L-1AlCl3��Һ��10%NH4F��Һ�������ϣ���ַ�Ӧ��μӰ�ˮ��������������AlCl3��NH4F��Ӧ�Ļ�ѧ����ʽΪAlCl3+NH4F=��NH4��3AlF6+3NH4Cl����ʵ�������Թܼ�ʢװNH4F��Һ���Լ�ƿ��Ϊ���ϲ��ʣ�ԭ���Ƿ�����еķ�����ˮ����������ᣬ������ܹ��벣���ж������跴Ӧ���Բ�����ǿ�ҵĸ�ʴ�Զ�����������ʴ�ԣ�
��4����ˮ�е�NO3-�����ཡ�������Σ����Ϊ�˽�������ˮ��NO3-��Ũ�ȣ����о���Ա�����ڼ��������������۽�NO3-��ԭΪN2���÷�Ӧ�����ӷ���ʽΪ10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O���˷�����ȱ���Ǵ������ˮ��������AlO2-����Ȼ���ܶ����ཡ������Σ��������Ҫ�Ը�����ˮ����һϵ�к���������
��֪��25��ʱ��Ksp[Al��OH��3]=1.3��10-33
Al��OH��3?AlO2-+H++H2O K=1.0��10-13
25��ʱ������ʹ�����������ˮ��AlO2-Ũ�Ƚ���1.0��10-6mol•L-1����Ӧ������pH=7����ʱˮ��c��Al3+��=1.3��10-12mol•L-1��
���� ��1���������ȷ�Ӧԭ��������������������Ӧ�����������ͷ���
��2������������Ӧ�������������۵�ߣ�����ˮ��Ӧ��������������������������Ļ�ѧ���ʱ�á����á���ԭ����ܹ����ܼ�����������ʹ�����治�����γ���������Ĥ��
��3���Ȼ��������立�Ӧ��������������狀��Ȼ�泥������ˮ����������ᣬ������ܹ��벣���ж������跴Ӧ��
��4�����������Ϣ����Ӧ��Ϊ������NO3-��OH-��������Ϊ��N2��H2O���������������μӷ�Ӧ�����ﻹ��AlO2-�����ݵ����غ��ԭ���غ���д����ʽ��
����Al��OH��3?AlO2-+H++H2O K=1.0��10-13�����ˮ��AlO2-Ũ�Ƚ���1.0��10-6mol•L-1������������Ũ�ȣ�����Ksp[Al��OH��3]=1.3��10-33������������Ũ�ȣ�
��� �⣺��1������������������Ӧ�����������ͷ�����ѧ����ʽ��V2O3+2Al$\frac{\underline{\;����\;}}{\;}$2V+Al2O3��
�ʴ�Ϊ��V2O3+2Al$\frac{\underline{\;����\;}}{\;}$2V+Al2O3��
��2������������Ӧ�������������۵�ߣ��������ھƾ��ƻ����ϼ����ۻ��������䣻����ˮ��Ӧ����������������������ѧ����ʽ��2Al+6H2O=2Al��OH��3+3H2����
�ʴ�Ϊ������������Ӧ�������������۵�ߣ�2Al+6H2O=2Al��OH��3+3H2�������治�����γ���������Ĥ��
��3���Ȼ��������立�Ӧ��������������狀��Ȼ�泥�����ʽ��AlCl3+NH4F=��NH4��3AlF6+3NH4Cl��������еķ�����ˮ����������ᣬ������ܹ��벣���ж������跴Ӧ���Բ�����ǿ�ҵĸ�ʴ�Զ�����������ʴ�ԣ����Ը�ʵ�������Թܼ�ʢװNH4F��Һ���Լ�ƿ��Ϊ���ϲ��ʣ�
�ʴ�Ϊ��AlCl3+NH4F=��NH4��3AlF6+3NH4Cl��������еķ�����ˮ����������ᣬ������ܹ��벣���ж������跴Ӧ���Բ�����ǿ�ҵĸ�ʴ�Զ�����������ʴ�ԣ�
��4�����������Ϣ����Ӧ��Ϊ������NO3-��OH-��������Ϊ��N2��H2O���������������μӷ�Ӧ�����ﻹ��AlO2-����Ӧ��Al��AlO2-��AlԪ�ػ��ϼ���0������Ϊ+3�ۣ�������3�ۣ�NO3-��N2������Ԫ�ػ��ϼ���+5�۽���Ϊ0�ۣ�������10�ۣ����ϼ�������С������Ϊ30������ԭ�Ӹ����غ㡢����غ㷴Ӧ�����ӷ���ʽ��10Al+6NO3-+4OH-=10AlO2-+3N2��+2H2O��
ˮ��AlO2-Ũ�Ƚ���1.0��10-6mol•L-1������Al��OH��3?AlO2-+H++H2O K=1.0��10-13����C��H+��=$\frac{1.0��1{0}^{-13}}{1.0��10{\;}^{-6}}$=10-7��mol/L����
pH=7��C��OH-��=10-7mol/L����25��ʱ��Ksp[Al��OH��3]=1.3��10-33����C��Al3+��=$\frac{1.3��10{\;}^{-33}}{��1{0}^{-7}��{\;}^{3}}$=1.3��10-12mol•L-1��
�ʴ�Ϊ��7��1.3��10-12mol•L-1��
���� ����Ϊ�ۺ��⣬�����˽�����ұ�������ӷ���ʽ������ʽ����д���й�ƽ�ⳣ���ļ��㣬��Ϥ�����仯���������ǽ���ؼ���ע�⻯ѧƽ�ⳣ����Ӧ�ã���Ŀ�Ѷ��еȣ�

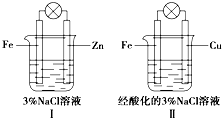
| A�� | ��͢��������������� | |
| B�� | ��͢��и�����Ӧ����Fe-2e-�TFe2+ | |
| C�� | ��͢���������Ӧ����O2+2H2O+4e-�T4OH- | |
| D�� | ��͢��е��ݾ��ᷢ�� |
| A�� | ������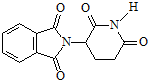 �ķ���ʽΪC13H9O4N2 �ķ���ʽΪC13H9O4N2 | |
| B�� | �ڼ��������£�CH3CO18OC2H5��ˮ�������CH3COOH��C2H518OH | |
| C�� | ��һ�������£����ᡢ�������ᡢ�����ʾ�����NaOH������Ӧ | |
| D�� | 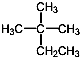 ��ϵͳ����Ϊ2-��-2-�һ����� ��ϵͳ����Ϊ2-��-2-�һ����� |
| A�� | ʳ���������ӵĽṹʾ��ͼΪ  | |
| B�� | ����������������ϡ��������ӷ���ʽ��FeO+2H+=Fe2++H2O | |
| C�� | NaHSˮ������ӷ���ʽ��HS-ʮH20?H3O++S2- | |
| D�� | �ö��Ե缫����Ȼ�����Һ�������缫��Ӧʽ��2Cl--2e-=Cl2�� |
| A�� | 2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ | B�� | I2+SO2+2H2O�TH2SO4+2HI | ||
| C�� | H2O2+H2SO4�TSO2+O2��+H2O | D�� | 2Fe3++2I-�T2Fe2++I2 |
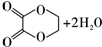 ��B�Ľṹ��ʽΪOGC-CHO��
��B�Ľṹ��ʽΪOGC-CHO��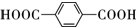
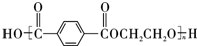 ��
��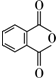 ��
��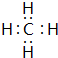 ��
�� �״���CH3OH����һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϣ���֪
�״���CH3OH����һ����Ҫ�Ļ���ԭ�ϣ��㷺Ӧ���ڻ���������Ҳ����ֱ������ȼ�ϣ���֪