题目内容
6.下列微粒的表示方法能够确定为氟离子的为( )| A. | X- | B. | 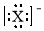 | C. | 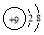 | D. | 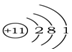 |
分析 氟离子的核电荷数为9、核外电子总数为10,最外层满足8电子稳定结构,据此进行判断.
解答 解:A.X-表示的是带有1个单位负电荷的离子,不一定为氟离子,故A错误;
B.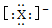 表示的是有1个单位负电荷的阴离子的电子式,可能为溴离子、氯离子,不一定为氟离子,故B错误;
表示的是有1个单位负电荷的阴离子的电子式,可能为溴离子、氯离子,不一定为氟离子,故B错误;
C.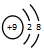 的核电荷数为9、核外电子总数为10,表示的是氟离子,故A正确;
的核电荷数为9、核外电子总数为10,表示的是氟离子,故A正确;
D. 质子数为11,表示的是钠原子结构示意图,故D错误;
质子数为11,表示的是钠原子结构示意图,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,明确常见化学用语表示的意义为解答关键,注意掌握离子结构示意图、电子式、阴阳离子的表示方法,试题培养了学生的规范答题能力.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
12. 短周期元素W、X、Y、Z的原子序数依次增加.甲、乙、丙、丁是由这些元素组成的二元化合物,乙为无色气体,丙为无色液体,丁为淡黄色固体.戊是元素Y的单质,是空气的主要成分,乙遇空气变红棕色,丁与丙反应有戊生成;己是元素Z的单质.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素W、X、Y、Z的原子序数依次增加.甲、乙、丙、丁是由这些元素组成的二元化合物,乙为无色气体,丙为无色液体,丁为淡黄色固体.戊是元素Y的单质,是空气的主要成分,乙遇空气变红棕色,丁与丙反应有戊生成;己是元素Z的单质.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.甲、乙、丙、丁是由这些元素组成的二元化合物,乙为无色气体,丙为无色液体,丁为淡黄色固体.戊是元素Y的单质,是空气的主要成分,乙遇空气变红棕色,丁与丙反应有戊生成;己是元素Z的单质.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素W、X、Y、Z的原子序数依次增加.甲、乙、丙、丁是由这些元素组成的二元化合物,乙为无色气体,丙为无色液体,丁为淡黄色固体.戊是元素Y的单质,是空气的主要成分,乙遇空气变红棕色,丁与丙反应有戊生成;己是元素Z的单质.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径Z>X>Y>W | B. | 丙的热稳定性不如甲 | ||
| C. | X的最高价氧化物的水化物为强酸 | D. | Z的最高价氧化物的水化物为强碱 |
14.下列依据实验目的所设计的实验操作中正确的是( )
| A. | 检验NaCl中含有Na2CO3,加水溶解 | |
| B. | 鉴别NaCl和Na2CO3溶液,加适量盐酸 | |
| C. | 除去CaO中的CaCO3,加足量稀盐酸 | |
| D. | 除去CO2中少量的CO,通入O2,点燃 |
1.由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法进行两组测定中和热的实验,实验试剂及其用量如表所示.
①甲在实验之前预计△H1=△H2.他的根据是A、B中酸与碱的元数、物质的量浓度、溶液体积都相同;乙在实验之前预计△H1≠△H2,他的根据是NaOH是强碱,NH3•H2O是弱碱电离吸热.
②实验测得的温度是:A的起始温度为13.0℃、终了温度为19.8℃;设充分反应后溶液的比热容c=4.184J/(g•℃),忽略实验仪器的比热容及溶液体积的变化,则△H1=-56.9kJ/mol.(已知溶液密度均为1g/cm3)
| 反应物 | 起始温度t1/℃ | 终了温度t2/℃ | 中和热/kJ•mol-1 |
| A.1.0mol/L HCl溶液50mL、1.1mol/L NaOH溶液50mL | 13.0 | △H1 | |
| B.1.0mol/L HCl溶液50mL、1.1mol/L NH3•H2O溶液50mL | 13.0 | △H2 |
②实验测得的温度是:A的起始温度为13.0℃、终了温度为19.8℃;设充分反应后溶液的比热容c=4.184J/(g•℃),忽略实验仪器的比热容及溶液体积的变化,则△H1=-56.9kJ/mol.(已知溶液密度均为1g/cm3)
11.设NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 1mol CaC2中有3NA个离子 | |
| B. | 1mol SiO2中含有2NA个共价键 | |
| C. | 1L 1mol/L CH3COONa溶液中含NA个CH3COO-离子 | |
| D. | 42g C2H4和C3H6的混合物中一定含有6NA个氢原子 |
16.元素单质及其化合物有广泛用途,请回答下列问题:
(1)第三周期元素中,钠原子核外有4种能量不同的电子;氯原子的最外层电子排布式为3S23p5;由这两种元素组成的化合物的电子式为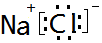 .
.
(2)下列气体能用浓硫酸干燥的是CD.
A.NH3 B.HI C.SO2 D.CO2
(3)请用一个实验事实说明钠与镁的金属性强弱与盐酸反应,钠的反应速率大,镁的反应速率慢.
(4)KClO3可用于实验室制O2,若不加催化剂,400℃时可分解生成两种盐,化学方程式为:KClO3$\stackrel{400℃}{→}$ KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为3:1.
(5)已知:
工业上电解MgCl2制单质镁,而不电解MgO的原因是MgO的熔点比MgCl2的熔点高,MgO熔融时耗费更多能源,增加成本.
(1)第三周期元素中,钠原子核外有4种能量不同的电子;氯原子的最外层电子排布式为3S23p5;由这两种元素组成的化合物的电子式为
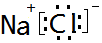 .
.(2)下列气体能用浓硫酸干燥的是CD.
A.NH3 B.HI C.SO2 D.CO2
(3)请用一个实验事实说明钠与镁的金属性强弱与盐酸反应,钠的反应速率大,镁的反应速率慢.
(4)KClO3可用于实验室制O2,若不加催化剂,400℃时可分解生成两种盐,化学方程式为:KClO3$\stackrel{400℃}{→}$ KCl+KClO4 (未配平),则氧化产物与还原产物的物质的量之比为3:1.
(5)已知:
| 化合物 | MgO | MgCl2 |
| 类型 | 离子化合物 | 离子化合物 |
| 熔点/℃ | 2800 | 714 |
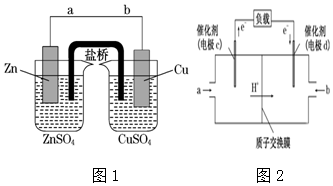
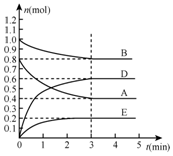 在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).
在某个容积为2L的密闭容器内,在T℃时按下图1所示发生反应:mA(g)+nB(g)?pC(g)+qE(s),△H<0(m、n、p、q为最简比例的整数).