题目内容
32g CO和CO2的混合气体,其体积在标准状况下为17.92L,求CO和CO2在标况下的体积分别是多少.
考点:物质的量的相关计算
专题:计算题
分析:CO和CO2混合气体的质量是32g、标况下混合气体体积为17.92L,根据气体质量和体积列方程组计算其组分体积.
解答:
解:设CO和CO2的物质的量分别是xmol、ymol,根据质量、体积列方程组得
,
解得
,
所以CO体积=0.2mol×22.4L/mol=4.48L,
二氧化碳体积=0.6mol×22.4L/mol=13.44L,
答:标况下,一氧化碳和二氧化碳体积分别是4.48L、13.44L.
|
解得
|
所以CO体积=0.2mol×22.4L/mol=4.48L,
二氧化碳体积=0.6mol×22.4L/mol=13.44L,
答:标况下,一氧化碳和二氧化碳体积分别是4.48L、13.44L.
点评:本题考查了物质的量的计算,根据m=nM、V=nVm进行计算即可,题目难度不大.

练习册系列答案
相关题目
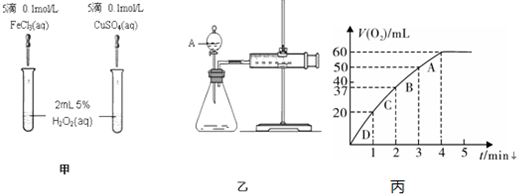
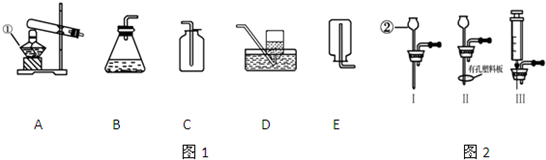

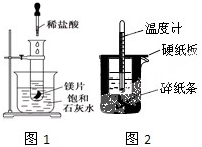 某学习小组设计以下实验,探究化学反应中的热效应.
某学习小组设计以下实验,探究化学反应中的热效应.