题目内容
3.在5L物质的量浓度为2mol/L的K2SO4溶液中K+的物质的量浓度为( )| A. | 4mol/L | B. | 5mol/L | C. | 1 mol/L | D. | 20mol/L |
分析 离子的浓度等于溶质的物质的量浓度×离子个数,以此来解答.
解答 解:物质的量浓度为2mol/L的K2SO4溶液中K+的物质的量浓度为2mol/L×2=4mol/L,
故选A.
点评 本题考查物质的量浓度的计算,为高频考点,把握溶质浓度与离子浓度的关系为解答的关键,侧重分析与计算能力的考查,注意与离子浓度与溶液的体积无关,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.氨水呈弱碱性的主要原因是( )
| A. | 通常情况下,氨的溶解度不大 | B. | 溶于水的氨分子只有少量电量 | ||
| C. | 氨水中的NH3•H2O电离出少量OH- | D. | 氨本身的碱性弱 |
1.下列离子方程式书写正确的是( )
| A. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═2Fe2++Fe3++4H2O | |
| B. | FeCl3溶液腐蚀铜线路板:Fe3++Cu=Cu2++Fe2+ | |
| C. | 金属铝加入到NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ |
18.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 60g SiO2中含有NA个SiO2分子 | |
| B. | 标况下,22.4L SO3的分子数为NA | |
| C. | 1L 0.5 mol•L-1 CuCl2溶液中含有0.5NA个Cu2+ | |
| D. | 15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.2NA |
5.已知:SO32-+I2+H2O═SO42-+2I-+2H+,某无色溶液中可能含有Na+、NH4+、Cu2+、K+、I-、SO32-、SO42-,且所有离子物质的量浓度相等.向溶液中滴加少量氯水,溶液呈无色(不考虑盐类的水解及水的电离).下列关于该溶液的判断正确的是( )
| A. | 肯定不含I- | B. | 不能确定是否含有SO42- | ||
| C. | 至少含有Na+、NH4+、K+中的两种 | D. | 可能含有Cu2+ |
8.下列说法正确的是( )
| A. | 2,5-二甲基己烷的核磁氢谱中出现三组峰 | |
| B. | 丙烷分子的比例模型: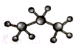 | |
| C. | 四氯化碳分子的电子式: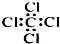 | |
| D. | 化合物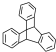 是苯的同系物 是苯的同系物 |
12.下列关于化学键叙述正确的是( )
| A. | 化学键是相邻原子间的相互作用 | |
| B. | 化学键既存在于相邻原子之间,又存在与相邻分子之间 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈互吸引作用 | |
| D. | 化学键通常是指物质中相邻的原子或离子之间存在的强烈相互作用 |