题目内容
甲、乙、丙、丁甲种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系、:甲
乙
丙.下列有关物质的推断不正确的是( )
| 丁 |
| 丁 |
| 甲 |
| A、若甲为焦炭,则丁可能是O2 |
| B、若甲为SO2,则丁可能是氨水 |
| C、若甲为NaAlO2溶液,则丁可能是盐酸 |
| D、若甲为CuCl2,则丁可能是氨水. |
考点:无机物的推断
专题:
分析:A.甲为焦炭,丁可能是O2,则乙为CO,丙为CO2;
B.若甲为SO2,丁为氨水,乙为亚硫酸氢铵,丙为亚硫酸铵;
C.若甲为NaAlO2,丁是可能是盐酸,则乙为氢氧化铝,丙为氯化铝;
D.甲为CuCl2,丁可能是氨水,则乙为氢氧化铜,氢氧化铜不能溶于氨水.
B.若甲为SO2,丁为氨水,乙为亚硫酸氢铵,丙为亚硫酸铵;
C.若甲为NaAlO2,丁是可能是盐酸,则乙为氢氧化铝,丙为氯化铝;
D.甲为CuCl2,丁可能是氨水,则乙为氢氧化铜,氢氧化铜不能溶于氨水.
解答:
解:A.甲为焦炭,则丁可能是O2,则乙为CO,丙为CO2,二氧化碳与C反应得到CO,符合转化关系,故A正确;
B.若甲为SO2,丁为氨水,乙为亚硫酸氢铵,丙为亚硫酸铵,亚硫酸铵与二氧化硫反应得到NH4HSO3,符合转化关系,故B正确;
C.若甲为NaAlO2,丁是可能是盐酸,则乙为氢氧化铝,丙为氯化铝,氢氧化铝和盐酸反应生成氯化铝,符合转化关系,故C正确;
D.甲为CuCl2,丁可能是氨水,则乙为氢氧化铜,氢氧化铜不能溶于氨水,不能反应生成丙,不符合转化关系,故D错误,
故选D.
B.若甲为SO2,丁为氨水,乙为亚硫酸氢铵,丙为亚硫酸铵,亚硫酸铵与二氧化硫反应得到NH4HSO3,符合转化关系,故B正确;
C.若甲为NaAlO2,丁是可能是盐酸,则乙为氢氧化铝,丙为氯化铝,氢氧化铝和盐酸反应生成氯化铝,符合转化关系,故C正确;
D.甲为CuCl2,丁可能是氨水,则乙为氢氧化铜,氢氧化铜不能溶于氨水,不能反应生成丙,不符合转化关系,故D错误,
故选D.
点评:本题考查无机物的推断,综合考查元素化合物性质,关键是掌握物质之间的相互转化,题目难度中等.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
下列说法不正确的是( )
| A、用石灰石或石灰乳进行燃煤烟气脱硫(除SO2)可获得副产品石膏 |
| B、金属的电化学防护措施有牺牲阳极的阴极保护法和外加电流的阴极保护法 |
| C、若在水里贮藏室中,放几块被KMnO4溶液浸透过的“砖块”,可延长水果保存时间 |
| D、常温时,某可逆反应的平衡常数越大则其反应速率就越快 |
下列说法正确的是( )
| A、工业制漂白粉是将氯气通入石灰水中制备 |
| B、海水中提取溴的方法是在经处理得到的含溴单质的水中鼓入热空气或水蒸气使溴单质挥发出来 |
| C、硫粉在过量的纯氧中燃烧可以生成三氧化硫 |
| D、少量二氧化碳通入氯化钙溶液中能生成白色沉淀 |
 常温下,向某浓度H2A溶液中逐滴加入一定量浓度NaOH溶液,所得溶液中H2A、HA-、A2-三种微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是( )
常温下,向某浓度H2A溶液中逐滴加入一定量浓度NaOH溶液,所得溶液中H2A、HA-、A2-三种微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是( )| A、H2A是一种二元弱酸 |
| B、常温下,H2A=H++HA-的电离平衡常数Ka1=0.01 |
| C、将相同物质的量的NaHA和Na2A固体溶于水所得混合溶液pH一定为5.5 |
| D、在量热计中,用20.0mL0.10mol/LnaOH溶液,分别与10.0mL0.20mol/LH2A和20.0mL0.10mol/LH2A反应后放出的热量不相同 |
下列各组数据中,其比值为2:1的是( )
| A、常温下,氨水与(NH4)2SO4溶液混合后pH=7的溶液中,c(NH4+):c(SO42-) |
| B、相同温度下,1 mol.L-1醋酸与0.5mol.L-1醋酸中c(H+)之比 |
| C、用同浓度盐酸中和相同体积pH均为12的Ba(OH)2和KOH,所需盐酸的体积之比 |
| D、pH=2的H2SO4溶液与pH=2的CH3COOH溶液中,c(CH3COOH):c(H2SO4) |
某混合溶液中可能含有下列离子中的若干种:NH4+、Na+、Al3+、Fe2+、AlO2-、SO42-、I-、NO3-、CO32-,已知离子浓度均为0.1mol.L-1.现取两份20mL该溶液进行如下实验:(1)第一份加入足量盐酸,产生气体在空气中变为红色,在反应后的溶液中加入BaCl2溶液,有白色沉淀产生.(2)第二份逐滴滴加NaOH浓溶液至过量,先产生沉淀不溶解,并有气体逸出.根据上述实验,以下说法错误的是( )
| A、该混合溶液汇总一定不含有Fe3+、AlO2-、Al3+、CO32- |
| B、在溶液中滴加酚酞试液后呈红色,加入BaCl2溶液,红色褪去,并产生白色沉淀 |
| C、该混合溶液中肯定含有Fe2+、NH4-、SO42-、NO3- |
| D、通过进行焰色反应可以确定是否含有I- |
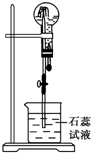 物质A是一种白色晶体,它与浓NaOH溶液共热,放出无色气体B,用圆底烧瓶收集干燥的B.按如图所示装置仪器,挤压滴管的胶头时,可以得到蓝色喷泉;A与浓硫酸反应,放出无色气体C,用圆底烧瓶收集干燥的C,仍按如图所示装置仪器,挤压滴管的胶头时,可以得到红色喷泉.
物质A是一种白色晶体,它与浓NaOH溶液共热,放出无色气体B,用圆底烧瓶收集干燥的B.按如图所示装置仪器,挤压滴管的胶头时,可以得到蓝色喷泉;A与浓硫酸反应,放出无色气体C,用圆底烧瓶收集干燥的C,仍按如图所示装置仪器,挤压滴管的胶头时,可以得到红色喷泉.