题目内容
20.下列说法正确的是( )| A. | 溶液、胶体、浊液的本质区别是分散质粒子直径的大小 | |
| B. | 生石灰与水混合的过程只发生物理变化 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | CuSO4•5H2O是一种混合物 |
分析 A.分散质粒子的大小不同是分散系的本质区别;
B.生石灰是氧化钙,与水混合发生反应生成氢氧化钙;
C.一种元素组成的纯净物为单质;
D.硫酸铜晶体是一种物质组成的纯净物.
解答 解:A.分散质粒子的大小不同是分散系的本质区别,分散质微粒直径,小于1nm的形成分散系为溶液,大于100nm为浊液,1-100nm的为胶体,故A正确;
B.生石灰与水混合的过程氧化钙与水混合发生反应生成氢氧化钙,过程中发生化学反应,故B错误;
C.O3是由3个氧原子构成的单质,故C错误;
D.CuSO4•5H2O是一种物质组成的纯净物,故D错误;
故选A.
点评 本题考查了胶体的性质、物质分类、物质组成分析判断,题目难度不大,掌握基础是解题关键.

练习册系列答案
相关题目
10.下列事实不能用勒夏特列原理解释的是( )
| A. | 对平衡体系H2(g)+I2(g)?2HI(g)加压后,混合气体的颜色加深 | |
| B. | 用稀盐酸洗涤AgCl沉淀比用等体积的蒸馏水洗涤损失的AgCl少 | |
| C. | 实验室可用排饱和食盐水是方法收集氯气 | |
| D. | 工业合成三氧化硫的过程中使用过量的氧气,以提高二氧化硫的转化率 |
8.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | CO2的电子式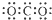 | B. | 质量数为37的氯原子${\;}_{37}^{17}$Cl | ||
| C. | 乙烯的结构简式C2H4 | D. | Cl-的结构示意图: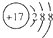 |
15.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | 石灰石与硝酸反应;石灰石与盐酸 | |
| B. | BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 | |
| C. | Na2CO3溶液与硝酸溶液;CaCO3溶液与硝酸溶液 | |
| D. | 氢氧化钠与盐酸,;氢氧化钠与碳酸 |
12.已知,常温常压下,过氧化钠(N2O2)是一种固体.标准状况下,等物质的量的N2O2和O2中相同的是( )
| A. | 两种物质中所含的氧原子数 | B. | 两种物质中所含的氧分子数 | ||
| C. | 两种物质的体积 | D. | 两种物质的质量 |
9.下列各组物质相互混合反应,既有气体生成,最终又一定有沉淀生成是( )
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
10.阿斯匹林的结构简式为: ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |