题目内容
8.下列反应中吸热反应的是( )| A. | 铝片与稀盐酸反应 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 氢氧化钠与稀盐酸反应 | D. | 甲烷在氧气中燃烧 |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸或与水、所有中和反应、绝大多数化合反应、铝热反应;
常见的吸热反应有:绝大数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气)还原金属氧化物、某些复分解(如铵盐和强碱),以此解答该题.
解答 解:A.为活泼金属与盐酸的反应,为放热反应,故A错误;
B.Ba(OH)2•8H2O与NH4Cl反应为吸热反应,故B正确;
C.酸碱中和反应为放热反应,故C错误;
D.有机物的燃烧为放热反应,故D错误.
故选B.
点评 本题考查化学反应中能量变化,为高频考点,侧重考查学生的分析能力,题目难度不大,掌握常见的放热反应和吸热反应是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),(银白色→变暗→表面变潮→结块→变成粉末).下列有关叙述中错误的是( )
| A. | 表面迅速变暗是因为钠与空气中的氧气反应生成了过氧化钠 | |
| B. | “出汗”是因为生成的氢氧化钠吸收空气中的CO2在表面形成了溶液 | |
| C. | 最后变成碳酸钠粉末 | |
| D. | 该过程中的所有化学反应均为氧化还原反应 |
16.下列有关浓硫酸的认识正确的是( )
| A. | 浓硫酸具有吸水性,可用来干燥H2S | B. | 浓硫酸在常温下不与铁和铝反应 | ||
| C. | 可将蒸馏水注入浓硫酸进行稀释 | D. | 棉花接触浓硫酸后会变黑 |
13.某温度时,a mol•L-1一元酸HA与b mol•L-1NaOH等体积混合后,pH为7,则下列说法正确的是( )
| A. | a<b | B. | a>b | ||
| C. | c (A-)=c(Na+) | D. | 以上情况都有可能 |
1.卤块的主要成分是MgCl2,此外还含Fe2+、Fe3+和Mn2+等杂质离子.以卤块为原料按图所示流程进行生产,可制得轻质氧化镁.
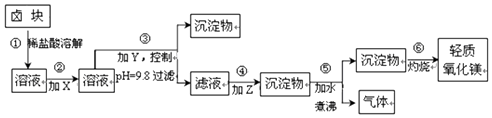
若要求产品尽量不含杂质且生产成本较低,请根据上表提供的资料回答:
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的acd( 选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)步骤③控制pH=9.8的目的是使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、坩埚和泥三角.

| 表1:生成氢氧化物沉淀的pH | 表2:原料价格表 | |||
| 物质 | 开始沉淀 | 沉淀完全 | 物质 | 价格(元/吨) |
| Fe(OH)3 | 2.7 | 3.7 | a.漂液(含25.2%NaClO) | 450 |
| Fe(OH)2 | 7.6 | 9.6﹡ | b.双氧水(含30%H2O2) | 2400 |
| 资*源%库Mn(OH)2 | 8.3 | 9.8 | c.烧碱(含98%NaOH) | 2100 |
| Mg(OH)2 | 9.6 | 11.1 | d.纯碱(含99.5%Na2CO3) | 600 |
(1)流程中加入的试剂X、Y、Z最佳选择依次是表2中的acd( 选填试剂编号).
(2)步骤②发生反应的离子方程式为2Fe2++ClO-+2H+=Cl-+2Fe3++H2O;步骤⑤中发生反应的化学方程为MgCO3+H2O $\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2↓+CO2↑.
(3)步骤③控制pH=9.8的目的是使除Mg2+以外的各种杂质金属离子都成为氢氧化物沉淀以便除去.
(4)若在实验室进行步骤⑥的灼烧实验,必须用到的仪器是铁三脚、酒精喷灯、坩埚和泥三角.
2.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论错误的是( )
| A. | 加入有色布条,一会儿有色布条褪色,证明溶液中有Cl2存在 | |
| B. | 向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl- | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 已知氧化性Cl2>Fe3+,向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有Cl2 |