题目内容
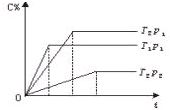 可逆反应:2A(g)+B(g)?2C(g)在温度分别为T1、T2,压强分别为p1、p2条件下测得C的体积分数与时间t的关系如图所示,下列判断正确的是:
可逆反应:2A(g)+B(g)?2C(g)在温度分别为T1、T2,压强分别为p1、p2条件下测得C的体积分数与时间t的关系如图所示,下列判断正确的是:( )
| A、p2<p1,逆反应放热 |
| B、p2>p1,正反应放热 |
| C、p2>p1,正反应吸热 |
| D、p2<p1,逆反应吸热 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:根据温度、压强对平衡移动的影响分析,温度越高、压强越大,则反应速率越大,达到平衡用的时间越少,曲线的斜率越大.
解答:
解:相同压强下,根据温度对反应速率的影响可知,温度越高,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:T2<T1,升高温度,C的含量减小,平衡向逆反应方向移动,则正反应为放热反应,逆反应吸热;
相同温度下,根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:P2<P1,压强越大,生成物C的物质的量越大,说明平衡向正反应方向移动,
故选D.
相同温度下,根据压强对反应速率的影响可知,压强越大,反应速率越大,则达到平衡用的时间越少,曲线的斜率越大,故有:P2<P1,压强越大,生成物C的物质的量越大,说明平衡向正反应方向移动,
故选D.
点评:本题考查了温度、压强对化学平衡的影响,根据“先拐先平数值大”确定温度、压强的相对大小,再结合温度、压强与生成物C物质的量的变化确定反应热及气体的计量数变化,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,甲酸的下列性质中,可以证明它是弱电解质的是( )
| A、甲酸能与水以任意比互溶 |
| B、1mol/L甲酸溶液的pH值约为2 |
| C、10ml 1mol/L甲酸恰好与10ml?1mol/L NaOH溶液完全反应 |
| D、HCOONa溶液的pH值大于7 |
设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A、0.1 mol/L NaHCO3和0.1 mol/L Na2CO3混合溶液1L,HCO3-,CO32-的总数为0.2NA |
| B、向密闭容器中充入2molN2和3molH2,在一定条件下发生反应,达到平衡时,混合气体中NH3的体积分数为23.45%,则H2和NH3所含的H原子总数为6NA |
| C、若1L0.1 mol/L的CH3COOH溶液含CH3COO- 数为aNA,则1L0.3 mol/L的CH3COOH溶液含CH3COO- 数小于0.3aNA |
| D、反应N2+3H2?2NH3达平衡时,每形成6NA个N-H键,也生成14克N2 |
下列装置能达到实验目的是( )
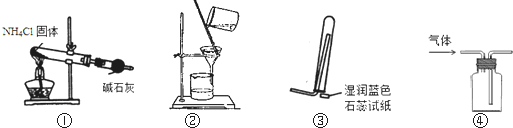

| A、用①装置制取干燥的氨气 |
| B、用②装置除去淀粉溶液中的NaCl |
| C、③装置可用于氨气的收集、检验 |
| D、④装置可用排空气法收集氢气 |
由乙烯和乙酸蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
| A、10% | B、20% |
| C、30% | D、无法确定 |
化学与科学、技术、社会、环境密切相关.下列有关说法中正确的是( )
| A、碳酸钡和硫酸钡均可用于钡餐透视 |
| B、为防止食物变质,可加入适量的食品添加剂 |
| C、浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 |
| D、海水淡化可以解决淡水危机,向海水中加入明矾可以使海水淡化 |
已知H2(g)+I2(g)?2HI(g),现有相同容积的体积可变的两个绝热容器甲和乙,甲中加入H2和I2各0.1mol,乙中加入HI 0.2mol,起始温度相同的条件下分别达到平衡.下列说法正确的是( )
| A、平衡时甲、乙两容器体积相等 |
| B、平衡时甲、乙两容器中c(H2)相等 |
| C、平衡时甲、乙两容器中反应速率v(H2)相等 |
| D、平衡时甲、乙两容器中气体总的物质的量相等 |